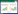文章信息
- 孙永红, 王文娇, 赵征宇, 蔡葵, 赵明
- SUN Yong-hong, WANG Wen-jiao, ZHAO Zheng-yu, CAI Kui, ZHAO Ming
- 生物质炭对茶园土壤水溶性氟吸附特性的影响
- Effects of Biochar on Adsorption Characteristics of Water-soluble Fluorine in Tea Garden Soil
- 农业资源与环境学报, 2017, 34(4): 376-383
- Journal of Agricultural Resources and Environment, 2017, 34(4): 376-383
- http://dx.doi.org/10.13254/j.jare.2017.0032
-
文章历史
- 收稿日期: 2016-02-09
氟是人体必需的微量矿质元素。人体摄入适量的氟可以维持骨骼和牙齿的正常生长和发育,防止血管老化。但过量摄入氟又会对人体产生氟斑牙、氟骨症等的危害[1]。茶树是一种氟富集能力强的植物,茶叶是茶树氟积累的主要器官[2]。近年来的研究表明,土壤水溶性氟含量与茶叶氟含量呈显著相关性,是影响茶叶氟含量的主要因素[3-5]。因此,降低土壤水溶性氟含量和高氟茶叶的质量安全风险,对保护饮茶者的健康具有重要的现实意义。
生物质炭(Biochar,BC)是由植物生物质在完全或部分缺氧条件下经热解炭化产生的一种高度芳香化的难熔性固态物质[6-7]。作为一种土壤改良剂,生物质炭不仅在改善土壤肥力、促进植物生长等方面具有重要的作用,而且因其具有多孔结构和炭表面丰富的含氧官能团,使得生物质炭具有较强的吸附能力,对土壤矿物质的迁移和生物有效性等具有重要的影响[8-11]。因此,将生物炭作为一种土壤原位修复材料,固定污染物并降低其生物有效性,修复受污染土壤,已成为农业生态环境研究的热点。已有研究表明,生物质炭对土壤NO3-、PO43-等具有强烈的吸附作用,并能影响Pb2+、Cd2+等重金属在环境中的迁移[12-16]。但关于生物质炭对茶园土壤中水溶性氟的吸附特性的影响研究未见报道。本研究以农业废弃物花生壳为原材料,在650 ℃裂解温度下制备生物质炭,并添加到茶园土壤中培养,分析研究施入生物质炭的土壤对水溶性氟的吸附特性,旨在为探讨施用生物质炭对茶园土壤水溶性氟的影响提供科学依据。
1-1 材料与方法1 试验材料1.1.1 供试土壤供试土壤采自青岛市农科院果茶所茶园,地处36°14′18″N,120°32′22″E,土壤采集深度0~20 cm。土壤母质为花岗岩坡积、洪积物,土壤类型为棕壤。土样经自然风干后,过0.25 mm筛备用。其基本性质为:有机质23.71 g·kg-1,pH(H2O)5.70,全氟401.4 mg·kg-1,水溶性氟0.84 mg·kg-1,交换性钾1.15 cmol·kg-1,交换性钠0.30 cmol·kg-1,交换性钙11.55 cmol·kg-1,交换性镁1.48 cmol·kg-1,阳离子交换量14.47 cmol·kg-1。
1.1.2 生物质炭供试生物质炭采用当地农业生产废弃的花生壳。将花生壳105 ℃烘干后粉碎过2 mm筛,装入瓷坩埚中压实、加盖,放入高温炉中逐渐升温至650 ℃炭化1 h,保温至自然冷却后取出,研磨过0.25 mm筛,密封保存备用。其基本性质为:有机碳436.5 g·kg-1,pH(H2O)9.55,全氟57.5 mg·kg-1,水溶性氟3.1 mg·kg-1,全氮23.75 g·kg-1,全磷2.41 g·kg-1,全钾23.75 g·kg-1,全钠3.50 g·kg-1,全钙5.40 g·kg-1,全镁6.48 g·kg-1,产出率29.2 %。
1.1.3 氟标准溶液准确称取经105 ℃烘干的氟化钠(NaF)2.210 0 g用去离子水溶解后定容至1 000 mL容量瓶中,配制成含氟1 000 mg·L-1标准贮备溶液。根据等温吸附试验设计分别配制氟含量为5、10、20、40、80、100 mg·L-1标准使用溶液,根据动力学试验设计配制氟含量为50 mg·L-1标准使用溶液。
1.2 试验方法1.2.1 土壤培养试验土壤培养试验设不添加生物质炭土壤(原土)和分别添加0.25%(T1)、0.50%(T2)、1.00%(T3)、2.00%(T4)生物质炭土壤共5个处理。分别称取200.00 g供试土壤,按试验设计加入生物质炭充分混匀后装入玻璃培养瓶中,加去离子水将土壤含水量调节至最大持水量的60%,放入25 ℃恒温培养箱培养30 d,期间加水调节土壤持水量1次。培养结束后将土壤取出风干、磨细过0.25 mm筛备用。各处理3次重复。
1.2.2 氟的等温吸附试验称取2.50 g培养土壤样品(W)于50 mL离心管中并称重(W1),分别加入氟含量为0、5、10、20、40、80、100 mg·L-1(Cx)标准溶液25 mL(V),加盖密封后置于25 ℃±1 ℃恒温振荡箱中以220 r·min-1振荡提取2 h,静止2 h,在4 000 r·min-1条件下离心5 min,分别吸取上清液测定氟浓度(C)。根据加入吸附液和吸附完成后平衡溶液的氟浓度之差再减去氟含量为0时的氟浓度(纯水,C0)计算土壤氟吸附量。
吸附量X(mg·kg-1)=(Cx -C-C0)×V/W
吸附率(%)=(吸附量×2.5)/(初始液氟浓度×25)×100
1.2.3 氟的等温解吸试验将上述试验倾出上清液的离心管称重(W2),然后加入去离子水25 mL,相同条件下振荡1 h,离心,吸取上清液测定氟浓度(C1)。根据吸附平衡液浓度和残留液体积计算氟的残留量,并从土壤解吸量减去,得土壤解吸量。
解吸量(mg·kg-1)=C1 × 25-C(W2-W1)/W
解吸率(%)=解吸量/吸附量×100
净吸附量(mg·kg-1)=吸附量-解吸量
1.2.4 氟的吸附动力学试验分别称取2.50 g培养土壤样品于50 mL离心管中,加入氟含量为50 mg·L-1标准溶液25 mL,加盖密封后置于25 ℃±1 ℃恒温振荡箱中以220 r·min-1振荡30、60、120、240、480、720 min和1 440 min后取出离心,吸取上清液测定氟浓度。
1.3 测定方法土壤水溶性氟含量采用土水比1:10恒温振荡1 h提取[17],生物质炭全氟采用Na2CO3-NaOH 600 ℃熔融提取,氟离子选择电极法测定[18];pH值采用电极电位法测定,土壤的土水比为1:2.5,生物质炭的炭水比为1:10;土壤阳离子交换量采用乙酸铵法测定;土壤交换性盐基采用乙酸铵提取,生物质炭矿质元素采用H2SO4-H2O2消解,分别用原子吸收分光光度法测定钙、镁含量,火焰光度法测定钾、钠含量;土壤有机质和生物质炭有机碳含量采用高温外热重铬酸钾-容量法测定;其他项目测定按常规方法进行[18]。
1.4 数据分析试验数据经SPSS 17.0和Microsoft Excel 2003分析软件进行数据统计和相关性分析,采用邓肯新复极差法进行多重比较。
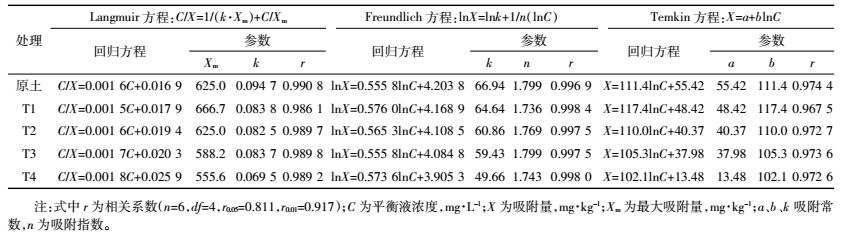
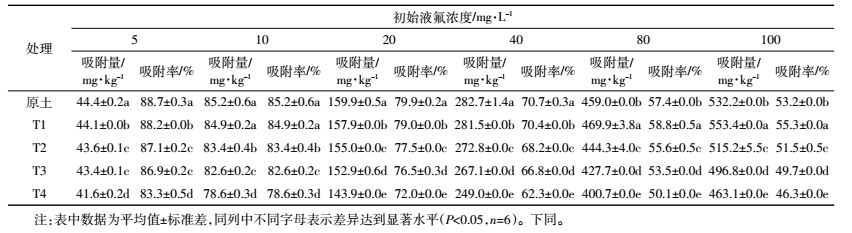
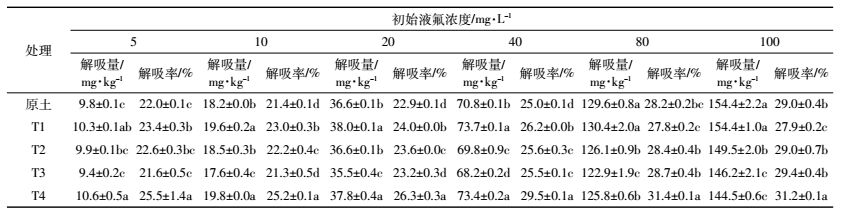
2 结果与讨论2.1 各试验处理土壤对水溶性氟吸附量和吸附率的影响各试验处理土壤水溶性氟的吸附量和吸附率见表 1。各试验处理土壤水溶性氟的吸附量随初始液氟浓度提高而增加。其中,添加生物质炭的T1~T4处理土壤在氟初始液浓度低于40 mg·L-1时(10 mg·L-1 T1处理除外)的氟吸附量显著低于原土(P<0.05),氟初始液浓度高于80 mg·L-1后的氟吸附量除T1处理土壤显著高于原土外,其他添加生物质炭处理的土壤均显著低于原土。添加生物质炭处理的土壤(T1~T4)随生物质炭添加量增加氟吸附量均显著降低,氟吸附量的大小顺序为:T1>T2>T3>T4。各试验处理土壤氟的等温吸附曲线见图 1。
 |
|
| 图 1 各试验处理土壤的氟等温吸附曲线 Figure 1 The isothermal adsorption curve of fluorine in soil |
各试验处理土壤的氟吸附率与氟吸附量相反,随初始液氟浓度提高各试验处理土壤的氟吸附率逐渐降低。添加生物质炭处理的土壤(T1~T4)在初始液氟浓度低于40 mg·L-1时(10 mg·L-1 T1处理除外)的氟吸附率显著低于原土,初始液氟浓度高于80 mg·L-1后的氟吸附率除T1显著高于原土外,其他添加生物质炭处理的土壤均显著低于原土。添加生物质炭处理的土壤(T1~T4)氟吸附率随生物质炭添加量的增加均显著降低,氟吸附率的大小顺序为:T1>T2>T3>T4。
等温吸附方程是描述吸附结果最常用的方法。本试验采用Langmuir方程、Freundlich方程和Temkin方程对各试验处理土壤水溶性氟吸附量与平衡液浓度进行拟合,结果见表 2。
根据Langmuir方程,分别以C/X对C作直线方程,求出Langmuir方程的最大吸附量Xm值和吸附常数k值。从拟合结果(表 2)看出,随生物质炭添加量的增加土壤对水溶性氟的最大吸附量逐渐降低,呈现T1>T2=原土>T3>T4趋势。吸附常数k值以原土最高,T1~T3处理土壤的k值差异不大,T4处理土壤的k值显著小于其他处理土壤。Langmuir方程的吸附常数k值与吸附结合力有关,k值越大意味着对离子的吸附能力也就越强,而生物质炭的加入降低了吸附常数k值,说明添加生物质炭降低了土壤对水溶性氟的吸附能力。
根据Freundlich方程,分别以lnX对lnC作直线方程,求出Freundlich方程中与吸附力有关的吸附常数k和n值。从拟合结果(表 2)看出,Freundlich方程的k值以原土最高,随着生物质炭添加量的增加k值逐渐降低,表示生物质炭添加量越大的土壤对初始液氟浓度的吸附量越小,表现为吸附曲线的截距降低。Freundlich方程中n为其中一个特征常数,一般认为当n>1时吸附容易进行,n=1时吸附是不可逆的,当n<0.5时表明该物质不易被吸附[19]。从表 2看出,各处理的n值均在1.7左右,处理间差异较小,说明添加生物质炭的土壤没有改变水溶性氟易被吸附的特性。
根据Temkin方程,分别以X对lnC作直线方程,求出Temkin方程常数a和b值(表 2)。其中,a值随着生物质炭添加量的增加而逐渐降低,T1~T4处理土壤b值随着生物质炭添加量的增加而降低。
从方程拟合曲线结果看出,Langmuir方程、Freundlich方程和Temkin方程的拟合相关性均在0.96以上,达到极显著水平,说明用Langmuir方程、Freundlich方程和Temkin方程均能够描述生物质炭加入茶园土壤后对水溶性氟的吸附规律,其中Freundlich方程拟合曲线的线性关系最佳,能更好地描述氟吸附过程[20]。而Langmuir方程和Temkin方程的拟合曲线分别呈现凸形状和凹形状,更符合二次函数曲线,如用直线方程解读氟吸附特性可能产生偏差。
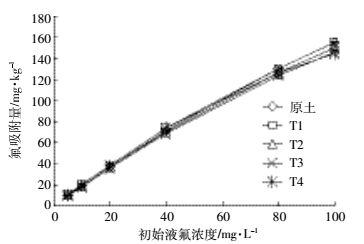
2.2 各试验处理土壤对水溶性氟解吸量和解吸率的影响各试验处理土壤氟解吸量随着初始液氟浓度提高而增加(表 3),处理间规律相同,差异量较小。当初始液氟浓度低于80 mg·L-1时,T1~T4处理土壤的解吸量呈现先降低后升高趋势。当氟初始液浓度达到100 mg·L-1时,T1~T4处理土壤的解吸量大小顺序为:T1>T2>T3>T4。与原土相比,T1处理土壤的氟解吸量始终高于原土,T3处理土壤的氟解吸量始终低于原土。T2处理土壤在初始液氟浓度低于40 mg·L-1时解吸量水平与原土基本相当,初始液氟浓度高于80 mg·L-1后氟解吸量开始低于原土。T4处理的土壤当初始液氟浓度低于40 mg·L-1时氟解吸量始终高于原土,当氟初始液浓度高于80 mg·L-1后氟解吸量开始低于原土。各处理土壤的解吸量与吸附量呈极显著正相关(r=0.996 1),但解吸量显著小于吸附量。各试验处理土壤的氟等温解吸曲线见图 2。
 |
|
| 图 2 各试验处理土壤氟的等温解吸曲线 Figure 2 The isothermal desorption curve of fluorine in soil |
各试验处理土壤解吸率在初始液氟浓度为10 mg·L-1时最低,初始液氟浓度在10~80 mg·L-1时氟解吸率逐渐升高,初始液氟浓度高于80 mg·L-1后解吸率变化趋于稳定。初始液氟浓度为100 mg·L-1时氟解吸率的大小顺序为T4>T3>T2=原土>T1。T4处理土壤氟解吸率始终显著高于其他处理土壤。
试验结果表明,土壤氟的吸附与解吸受初始液氟浓度的控制,随氟初始液浓度的增加,吸附量和解吸量也不断增加,直至达到最大值,这两种变化控制着土壤氟的净吸附量。刘忠翰[21]研究报道,土壤吸附氟的解吸特征极为重要,其能力大小影响土壤氟环境容量,因此衡量土壤氟保持容量更宜用净吸附量。从图 3看出,土壤氟净吸附量随初始液氟浓度的增加而增加,当初始液氟浓度低于40 mg·L-1时T1~T4处理土壤的氟净吸附量小于原土;初始液氟浓度高于80 mg·L-1后T1处理土壤的氟净吸附量大于原土,而T2~T4处理土壤则仍然小于原土。不同初始液氟浓度处理的T1~T4土壤氟净吸附量均随生物质炭添加量的增加而逐渐降低。

|
| 图 3 各试验处理土壤的氟净吸附量 Figure 3 The net adsorption of fluoride in soil |
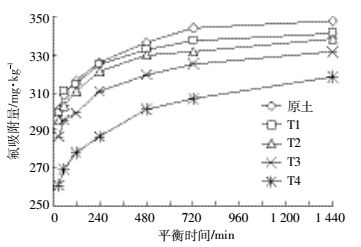
各试验处理土壤的水溶性氟吸附动力学曲线显示(图 4),水溶性氟的吸附量与平衡时间有关,吸附动力学过程包含吸附快反应和慢反应阶段,各处理土壤有基本相同的规律,即随着吸附平衡时间的延长,氟吸附量逐渐增大。其中,小于120 min平衡时间区间氟吸附量增加较快,随平衡时间再继续延长各处理的氟吸附量增加幅度逐渐变缓,达到1 440 min后T1、T2和原土处理基本达到平衡状态。平衡120 min时各处理吸附量占平衡1 440 min时吸附量的百分比分别为:原土90.8 %、T1 91.9 %、T2 91.7 %、T3 90.0 %和T4 87.3 %。
|
| 图 4 各试验处理土壤吸附动力学曲线 Figure 4 The adsorption dynamics curves of soil |
从不同平衡时间各处理土壤氟吸附量(图 4)看出,添加生物质炭处理的土壤氟吸附量始终低于原土,而且随着生物质炭添加量的增加,各处理土壤氟吸附量均明显降低,氟吸附曲线截距降低,吸附平衡时间延迟。
为进一步研究添加生物质炭土壤对水溶性氟的吸附动力学特性,本文应用双常数方程、Elovich方程、一级动力学方程、二级动力学方程和抛物线方程对各处理水溶性氟动力学曲线进行拟合[22]。结果表明(表 4),双常数方程、Elovich方程、一级动力学方程的非线性拟合决定系数(R2)均大于0.96,拟合性较好。拟合方程中,在反应进行初期,a值越大的土壤其氟吸附速率越大,b值越大的土壤吸附速率越小[23]。采用双常数方程、Elovich方程和一级动力学方程拟合方程计算得到的理论吸附量与试验实测吸附量之间的符合程度较高,方程的a值和b值也与试验结果基本吻合,可准确描述添加生物质炭土壤对水溶性氟的吸附过程。而二级动力学方程和抛物线方程计算得到的理论吸附量与试验实测吸附量之间的符合程度差异较大,不适用于添加生物质炭土壤对水溶性氟的吸附动力学研究。试验说明,添加生物质炭的土壤对水溶性氟的吸附并非呈单分子层分布,可能包含了吸附、扩散、溶解、矿化等复杂的反应过程综合作用的结果[24-25]。
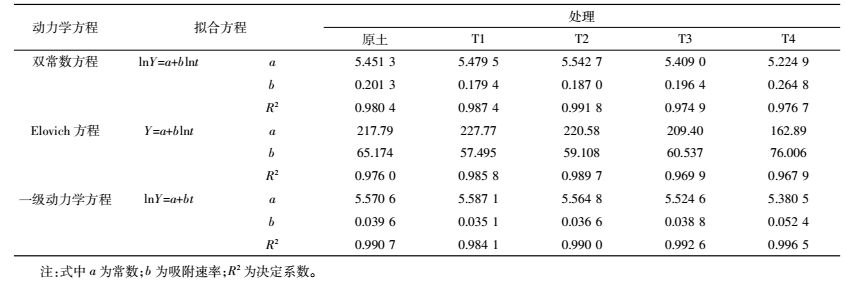 |
在1 440 min的平衡时间内,T1~T4处理土壤的氟吸附速率(b值)随生物质炭添加量的增加而提高,表明随生物质炭添加量的增加土壤的吸附速率降低。供试各处理土壤中,T1~T3处理土壤的氟吸附速率大于原土,T4处理土壤的氟吸附速率小于原土,说明添加生物质炭大于1.00 %后的土壤氟吸附速率将低于原土。
2.4 土壤pH值变化对土壤水溶性氟吸附特性的影响已有研究表明,土壤pH值、有机质、粘粒以及Fe、Al、Mn氧化物等对氟的吸附会产生较大的影响,而且土壤对氟离子的吸附属专性吸附,其吸附量随pH值升高而降低[26-28]。由于生物质炭含有的矿质元素如Na、K、Mg、Ca等以氧化物或碳酸盐的形式存在于灰分中,遇水后呈碱性[29],添加到土壤后可改变原有土壤的部分化学性质,并对水溶性氟的吸附特性产生影响。本试验中T1~T4处理土壤的pH值分别为5.74、5.81、5.91和6.18(表 5),比原土分别提高了0.04、0.11、0.21个和0.48个单位,随生物质炭添加量的增加土壤pH值逐渐提高。从表 5看出,T1~T4处理土壤的pH值与等温吸附Langmuir方程中的最大氟吸附量(Xm)、Freundlich方程中的吸附常数k值、Temkin方程中的吸附常数b值和氟平均净吸附量均呈二次函数关系,拟合度较好(R2>0.98)。
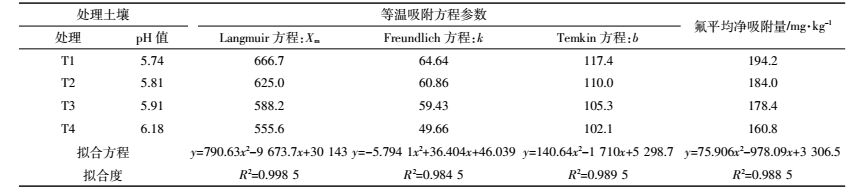 |
上述拟合参数随土壤添加生物质炭后pH值的提高而降低,其原因可能是通过生物质炭引入的OH-易与原土壤中和由生物质炭添加而带入的Ca2+、Fe3+、Al3+等金属氧化物生成沉淀,减少或抑制了与F-的交换反应[30-32]。添加生物质炭使土壤pH值升高与茶园土壤对水溶性氟最大吸附量、吸附强度和净吸附量的降低密切相关,生物质炭的其他影响因素有待进一步研究。
3 结论(1)各试验处理土壤氟吸附量随着初始液氟浓度提高而增加,随生物质炭添加量的增加土壤氟吸附量和吸附率均逐渐降低。应用等温吸附Langmuir方程、Freundlich方程和Temkin方程均能够较好地描述生物质炭加入茶园土壤后对水溶性氟的吸附规律,其中Freundlich方程拟合曲线的线性关系最佳,能更好地描述氟吸附过程。
(2)各试验处理土壤氟解吸量随着初始液氟浓度提高而增加,处理间规律相同,差异量较小。2 %生物质炭添加量处理土壤的氟解吸率始终显著高于其他处理土壤。各处理土壤的解吸量与吸附量呈极显著正相关,但解吸量显著小于吸附量。随生物质炭添加量的增加土壤氟净吸附量逐渐降低。
(3)各处理土壤的氟吸附动力学曲线有基本相同的规律,即随着吸附平衡时间的延长,氟吸附量逐渐增大,平衡时间小于120 min区间吸附量快速增加,平衡时间达到1 440 min后0.25 %和0.50 %生物质炭添加量处理土壤基本达到平衡状态。随着生物质炭添加量的增加,氟吸附动力学曲线截距降低,氟吸附平衡时间延迟。采用双常数方程、Elovich方程和一级动力学方程拟合方程计算得到的理论吸附量与试验实测吸附量之间的符合程度较高,方程的a值和b值也与试验结果基本吻合,可准确描述添加生物质炭土壤对水溶性氟的吸附过程。
(4)不同生物质炭处理的土壤pH值随生物质炭添加量的增加而提高,与等温吸附Langmuir方程中的最大氟吸附量(Xm)、Freundlich方程中的吸附常数k值、Temkin方程中的吸附常数b值和氟平均净吸附量呈二次函数关系,拟合结果均随土壤pH值的提高而降低,说明添加生物质炭使土壤pH值升高与茶园土壤对水溶性氟最大吸附量、吸附强度和净吸附量的降低密切相关。
| [1] | 李静, 谢正苗, 徐建明. 我国氟的土壤环境质量指标与人体健康关系的研究概况[J]. 土壤通报, 2006, 37(1): 194–199. LI Jing, XIE Zheng-miao, XU Jian-ming. Research progress in the relationship between soil environmental quality index of fluorine and human health in China[J]. Chinese Journal of Soil Science, 2006, 37(1): 194–199. (in Chinese) |
| [2] | 沙济琴, 郑达贤. 福建茶树鲜叶含氟量的研究[J]. 茶叶科学, 1994, 14(1): 37–42. SHA Ji-qin, ZHENG Da-xian. Study on fluorine content of fresh tea leaves in Fujian[J]. Journal of Tea Science, 1994, 14(1): 37–42. (in Chinese) |
| [3] | 马立锋, 阮建云, 石元值, 等. 中国茶叶中的氟近十年来的研究进展[J]. 生态环境, 2003, 12(3): 342–345. MA Li-feng, RUAN Jian-yun, SHI Yuan-zhi, et al. Review of the study on fluorine status in teas from China in the past decade[J]. Ecology and Environment, 2003, 12(3): 342–345. (in Chinese) |
| [4] | 阮建云, 杨亚军, 马立锋. 茶叶氟研究进展:累积特性、含量及安全性评价[J]. 茶叶科学, 2007, 27(1): 1–7. RUAN Jian-yun, YANG Ya-jun, MA Li-feng. Recent progress in the research on fluoride in tea:Accumulation characteristics by plants and concentrations in products with regarding to the impact on human health[J]. Journal of Tea Science, 2007, 27(1): 1–7. (in Chinese) |
| [5] | 赵明, 蔡葵, 王文娇, 等. 土壤交换性能与茶叶氟化物含量的相关性及其影响因素[J]. 农业资源与环境学报, 2016, 33(3): 276–280. ZHAO Ming, CAI Kui, WANG Wen-jiao, et al. Correlation between soil exchange properties and fluoride content in tea and its affecting factors[J]. Journal of Agricultural Resources and Environment, 2016, 33(3): 276–280. (in Chinese) |
| [6] | Sohi S P, Krull E, Lopez-Capel E, et al. A review of biochar and its use and function in soil[J]. Advances in Agronomy, 2010, 105: 47–82. DOI:10.1016/S0065-2113(10)05002-9 |
| [7] | Zhang L H, Xu C B, Champagne P. Overview of recent advances in thermo-chemical conversion of biomass[J]. Energy Conversion and Management, 2010, 51: 969–982. DOI:10.1016/j.enconman.2009.11.038 |
| [8] | 袁金华, 徐仁扣. 生物质炭的性质及其对土壤环境功能影响的研究进展[J]. 生态环境学报, 2011, 20(4): 779–785. YUAN Jin-hua, XU Ren-kou. Progress of the research on the properties of biochars and their influence on soil environmental functions[J]. Ecology and Environmental Sciences, 2011, 20(4): 779–785. (in Chinese) |
| [9] | Middelburg J J, Nieuwenhuize J, van Breugel P. Black carbon in marine sediments[J]. Marine Chemistry, 1999, 65: 245–252. DOI:10.1016/S0304-4203(99)00005-5 |
| [10] | Glaser B, Haumaier L, Guggenberger G, et al. Black carbon in soils:The use of benzene carboxylic acids as specificmarkers[J]. Organic Geochemistry, 1998, 29: 811–819. DOI:10.1016/S0146-6380(98)00194-6 |
| [11] | Liang B, Lehmann J, Solomon D, et al. Black carbon increases cation exchange capacity in soils[J]. Soil Sci Soc Am J, 2006, 70(5): 1719–1730. DOI:10.2136/sssaj2005.0383 |
| [12] | 王冰, 赵闪闪, 秦治家, 等. 生物质炭对黑土吸附-解吸硝态氮性能的影响[J]. 农业环境科学学报, 2016, 35(1): 115–121. WANG Bing, ZHAO Shan-shan, QIN Zhi-jia, et al. Effect of biochar on adsorption-desorption characteristics of nitrate nitrogen in black soil[J]. Journal of Agro-Environment Science, 2016, 35(1): 115–121. DOI:10.11654/jaes.2016.01.016(in Chinese) |
| [13] | 潘逸凡, 杨敏, 董达, 等. 生物质炭对土壤氮素循环的影响及其机理研究进展[J]. 应用生态学报, 2013, 24(9): 2666–2673. PAN Yi-fan, YANG Min, DONG Da, et al. Effects of biochar on soil nitrogen cycle and related mechanisms:A review[J]. Chinese Journal of Applied Ecology, 2013, 24(9): 2666–2673. (in Chinese) |
| [14] | 黄容, 高明, 廖燕妮. 不同生物质灰渣对磷的吸附解吸动力学特征[J]. 水土保持学报, 2014, 28(1): 156–160. HUANG Rong, GAO Ming, LIAO Yan-ni. Phosphorus adsorption and desorption kinetics capacity of different biomass ash[J]. Journal of Soil and Water Conservation, 2014, 28(1): 156–160. (in Chinese) |
| [15] | 刘莹莹, 秦海芝, 李恋卿, 等. 不同作物原料热裂解生物质炭对溶液中Cd2+和Pb2+的吸附特性[J]. 生态环境学报, 2012, 21(1): 146–152. LIU Ying-ying, QIN Hai-zhi, LI Lian-qing, et al. Adsorption of Cd2+and Pb2+ in aqueous solution by biochars produced from the pyrolysis of different crop feedstock[J]. Ecology and Environmental Sciences, 2012, 21(1): 146–152. (in Chinese) |
| [16] | 蒋田雨, 姜军, 徐仁扣, 等. 稻草生物质炭对3种可变电荷土壤吸附Cd(Ⅱ)的影响[J]. 农业环境科学学报, 2012, 31(6): 1111–1117. JIANG Tian-yu, JIANG Jun, XU Ren-kou, et al. Effect of biochar from rice straw on adsorption of Cd(Ⅱ) by variable charge soils[J]. Journal of Agro-Environment Science, 2012, 31(6): 1111–1117. (in Chinese) |
| [17] | 徐为霞, 林珍珠, 高树芳, 等. 酸性土壤有效氟提取方法的研究[J]. 农业环境科学学报, 2006, 25(5): 1388–1392. XU Wei-xia, LIN Zhen-zhu, GAO Shu-fang, et al. Extraction method for available fluorine in acid soils[J]. Journal of Agro-Environment Science, 2006, 25(5): 1388–1392. (in Chinese) |
| [18] | 鲁如坤. 土壤农业化学分析方法[M]. 北京: 中国农业科技出版社, 2000: 22-34. LU Ru-kun. Analysis method of soil agricultural chemistry[M]. Beijing: China Agricultural Science and Technology Press, 2000: 22-34. (in Chinese) |
| [19] | 王静, 雷宏杰, 邱珍珍, 等. 大孔树脂对红枣汁中棒曲霉素的吸附动力学[J]. 农业工程学报, 2015, 31(23): 285–291. WANG Jing, LEI Hong-jie, QIU Zhen-zhen, et al. Adsorption characteristics of patulin in jujube juice using macroporous resin[J]. Transactions of the Chinese Society of Agricultural Engineering, 2015, 31(23): 285–291. DOI:10.11975/j.issn.1002-6819.2015.23.038(in Chinese) |
| [20] | 焦有. 土壤的氟吸附特性及影响因素[J]. 土壤通报, 1997, 28(3): 116–118. JIAO You. Adsorption characteristics of fluorine in soil and influencing factors[J]. Chinese Journal of Soil Science, 1997, 28(3): 116–118. (in Chinese) |
| [21] | 刘忠翰. 红壤氟保持容量的研究[J]. 土壤学报, 1988, 25(3): 236–242. LIU Zhong-han. Study of fluorine retention capacity of red earths[J]. Acta Pedologica Sinica, 1988, 25(3): 236–242. (in Chinese) |
| [22] | 谢忠雷, 刘磊, 侯赞梅, 等. 氟铝交互作用对茶园土壤氟吸附动力学特征的影响[J]. 吉林大学学报(地球科学版), 2006, 36(增刊): 154–158. XIE Zhong-lei, LIU Lei, HOU Zan-mei, et al. Effects of interaction of fluoride and aluminum on the characteristics of adsorption-kinetics of fluoride in tea garden soil[J]. Journal of Jilin University(Earth Science Edition), 2006, 36(Suppl): 154–158. (in Chinese) |
| [23] | 涂从. 土壤体系中的化学动力学方程及其应用[J]. 热带亚热带土壤科学, 1994, 3(3): 175–182. TU Cong. Equations of chemical kinetics and their application to soil system[J]. Tropical and Subtropical Soil Science, 1994, 3(3): 175–182. (in Chinese) |
| [24] | 杨军耀. 土壤氟吸附动力学模型[J]. 土壤通报, 1997, 28(6): 283–284. YANG Jun-yao. Kinetic model of soil fluorine adsorption[J]. Chinese Journal of Soil Science, 1997, 28(6): 283–284. (in Chinese) |
| [25] | 魏志远, 黎成厚, 漆智平. 几种土壤氟吸附动力学研究[J]. 土壤通报, 2006, 37(4): 720–722. WEI Zhi-yuan, LI Cheng-hou, QI Zhi-ping. Kinetics of fluorine adsorption in several soils[J]. Chinese Journal of Soil Science, 2006, 37(4): 720–722. (in Chinese) |
| [26] | 魏世勇. 湖北恩施几种典型土壤对氟的吸附与解吸特性[J]. 土壤通报, 2008, 39(1): 71–75. WEI Shi-yong. Adsorption and desorption characters of fluoride by several soils of Enshi[J]. Chinese Journal of Soil Science, 2008, 39(1): 71–75. (in Chinese) |
| [27] | 阮建云, 马立锋, 石元值, 等. 茶园土壤对氟的吸附与解吸特性[J]. 茶叶科学, 2001, 21(2): 161–165. RUAN Jian-yun, MA Li-feng, SHI Yuan-zhi, et al. Adsorption and desorption of fluoride by tea soils[J]. Journal of Tea Science, 2001, 21(2): 161–165. (in Chinese) |
| [28] | 徐明岗. 土壤离子吸附1.离子吸附的类型及研究方法[J]. 中国土壤与肥料, 1997, 5: 3–7. XU Ming-gang. oil adsorption 1. Types and methods of ion adsorption[J]. Soils and Fertilizers, 1997, 5: 3–7. (in Chinese) |
| [29] | 谢祖彬, 刘琦, 许燕萍, 等. 生物炭研究进展及其研究方向[J]. 土壤, 2011, 43(6): 857–861. XIE Zu-bin, LIU Qi, XU Yan-ping, et al. Advances and perspectives of biochar research[J]. Soils, 2011, 43(6): 857–861. (in Chinese) |
| [30] | 李日邦. 土壤吸附氟的能力及其生态学意义[J]. 环境科学学报, 1991, 11(3): 263–268. LI Ri-bang. Adsorption of fluoride soils and its ecological significance[J]. Acta Scientiae Circumstantiae, 1991, 11(3): 263–268. (in Chinese) |
| [31] | 谢正苗, 吴卫红, 徐建民. 环境中氟化物的迁移和转化及其生态效应[J]. 环境科学进展, 1999, 7(2): 40–53. XIE Zheng-miao, WU Wei-hong, XU Jian-min. Translocation and transformation of fluorides in the environment and their biological effects[J]. Environmental Science Progress, 1999, 7(2): 40–53. (in Chinese) |
| [32] | 万红友, 黎成厚, 师会勤, 等. 几种土壤的氟吸附特性研究[J]. 农业环境科学学报, 2003, 22(3): 329–332. WAN Hong-you, LI Cheng-hou, SHI Hui-qin, et al. Study on adsorption characters of fluorine in several soils[J]. Journal of Agro-Environment Science, 2003, 22(3): 329–332. (in Chinese) |
 2017, Vol. 34
2017, Vol. 34