文章信息
- 傅成锴, 郭千里, 梁成博, 郭子彰, 张成禄
- FU Cheng-kai, GUO Qian-li, LIANG Cheng-bo, GUO Zi-zhang, ZHANG Cheng-lu
- 高酸度芦苇活性炭的制备及其吸附性能
- Preparation and Adsorption Performances of Phragmites australis Activated Carbon with High Acidity
- 农业资源与环境学报, 2017, 34(2): 175-181
- Journal of Agricultural Resources and Environment, 2017, 34(2): 175-181
- http://dx.doi.org/10.13254/j.jare.2016.0275
-
文章历史
- 收稿日期: 2016-11-16
2. 济南市历城第二中学, 山东 济南 250104;
3. 日照市新营中学, 山东 日照 276826;
4. 中铁十四局集团有限公司, 山东 济南 250000
2. Jinan Licheng No.2 High School, Jinan 250104, China;
3. Rizhao Xinying Middle School, Rizhao 276826, China;
4. China Railway 14 th Construction Bureau Co Ltd, Jinan 250000, China
水体是生态环境的重要组成部分,亦是人类赖以生存的自然资源。由于人类活动的影响,特别是采矿、电镀、电子、化工、冶炼等工业的发展,大量的重金属排入水体中造成严重的污染。重金属在水体中积累到一定的程度就会对水体-水生植物-水生动物系统产生严重危害,并可能通过食物链直接或间接地影响到人类的健康[1-2]。然而,重金属由于很高的稳定性及难降解性,其造成的水体污染难以治理,因此水体重金属污染已经成为当今世界上最严重的环境问题之一。在众多水体重金属污染的处理方法中,活性炭(AC)吸附法由于其良好的处理效果以及简易的操作流程被广泛采用[3-4]。活性炭作为高效的吸附剂主要是由于其具备发达的孔径结构、较大的比表面积以及丰富的表面官能团[5-7]。研究表明,在重金属废水处理的过程中,活性炭的表面化学作用起主要作用,并且提高活性炭的表面酸度有利于水体中重金属离子的吸附作用[8]。
芦苇(Phragmites australies, PA),是人工湿地中常见的植物,常作为原料生产高性能活性炭。其制备方法主要有物理活化法和化学活化法。其中,化学活化法更容易调控活性炭的表面化学性质,常用的活化剂有磷酸、氢氧化钾、氯化锌等。磷酸法由于其所需活化温度低,产率高等优点,在工业生产中得到广泛的应用。为了进一步提高活性炭的理化性质和吸附能力,研究人员开发了很多改性方法,比如热收缩法、微波法、表面氧化法、表面还原法、金属离子负载等方法。针对提高活性炭的表面酸度可以有效地改善对水中重金属离子的吸附能力,有研究者使用H2O2、HNO3对活性炭进行表面处理来提高酸度[9];更有研究者在活化过程中原位掺杂有机酸进行改性[10];还有研究者通过开发像磷酸酯类等新型活化剂来提高活性炭表面酸度[11]。这些改性方法都集中在活性炭制备过程的中、后段。然而,对于活性炭制备过程前段的原料处理环节的改性鲜有报道。
本文提出一种活性炭制备过程中能够有效提高活性炭表面酸度的原料预处理方法--青贮活化法。秸秆青贮一方面能够有效地使秸秆质地变软,从而使活化剂更充分地利用,提高浸渍效果;另一方面能够大幅增加原料中的有机酸含量,从而提高所制备活性炭的表面酸度[12]。本文的主要研究目的:(1)评价青贮活化法的制备活性炭的可行性;(2)通过对比常规磷酸法制备的活性炭,系统调查青贮活化法制备活性炭的理化性质;(3)探究所制备的高酸度活性炭对重金属离子Ni(Ⅱ)和Cd(Ⅱ)的吸附性能。
1 材料与方法 1.1 试剂与仪器芦苇秸秆(取自山东济宁南四湖人工湿地),磷酸(85%),氯化镍、氯化镉、硝酸铅、盐酸、氢氧化钾等,以及其他相关化学试剂皆为分析纯,购自国药集团化学试剂有限公司。
pHs-3C型精密pH计(上海雷磁仪器厂);火焰原子吸收分光光度计(180-80,Hitachi,Japan)。
1.2 活性炭的制备 1.2.1 芦苇秸秆青贮处理将芦苇秸秆剪短至2~3 cm,喷洒一定量的水,控制秸秆含水率在50%~60%。秸秆放入泡菜罐中,压实、密封,进行青贮,3、5、7、14 d后取出,记为PA-3、PA-5、PA-7、PA-14,储存、备用。装置如图 1所示。

|
| 图 1 芦苇秸秆青贮处理示意图 Figure 1 he schematic of silage-treated method of Phragmites australis |
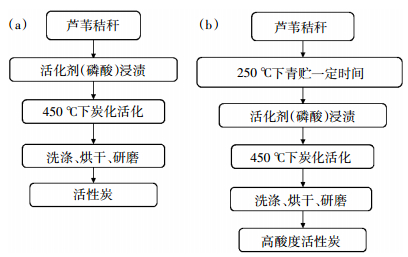
将青贮处理后的芦苇秸秆清洗干燥并粉碎至40~100目,称取10 g于烧杯中,加入20 g磷酸溶液,搅拌、混匀,室温下浸渍10 h。将浸渍后的样品转移到坩埚中,放入马弗炉中在450 ℃下炭化活化1 h。待温度降至100 ℃以下,取出样品,反复洗涤至pH稳定。然后研磨至160~200目,存储、备用。青贮芦苇秸秆PA-3、PA-5、PA-7、PA-14处理后分别记为AC-3、AC-5、AC-7、AC-14。将未青贮处理的芦苇秸秆按上述步骤制备活性炭作为对比(AC),来探讨青贮活化法的可行性。制备流程如图 2所示。
|
| 图 2 活性炭传统制备方法(a)和高酸度活性炭青贮活化法(b)制备流程图 Figure 2 Schematic representation of the conventional route (a) and the silage-treated route for the AC preparation (b) |
采用X射线衍射仪(XRD,Philips Electronic Instruments)测定芦苇原料及青贮后的结构形态。
采用扫描电镜(SEM,JEOL,JSM7600F,Japan)观察芦苇青贮前后的表面形貌。
采用元素分析仪(Vario EI Ⅲ Element Analyzer,USA)测定芦苇原料以及活性炭中C、H、O、N含量(质量分数)。
采用孔径分析仪(Quantachrome Corporation,USA)于77 K下测定氮气的吸附等温线。由BET多点法计算活性炭的比表面积(SBET),活性炭的微孔比表面积(Smic)和微孔孔径(Vmic)使用t-plot方法计算,在P/P0=0.99下确定总孔容(Vtot)的大小。使用DFT理论计算活性炭的孔径分布。平均孔径(Dp)大小由Dp=4Vtot /SBET计算得出。
采用Boehm滴定的方法测定活性炭的官能团含量,具体操作方法如文献[13]所述。酸性官能团含量的计算基于以下假设:NaOH中和羧基(Carboxyl)、内脂基(Lactone)和酚羟基(Phenolic),Na2CO3中和羧基和内脂基,NaHCO3中和羧基。故活性炭的羧基数量用NaHCO3的碱消耗量表示(mmol·g-1),内脂基数量用Na2CO3和NaHCO3碱消耗量之差表示(mmol·g-1),酚羟基数量用NaOH和Na2CO3的碱消耗量之差表示(mmol·g-1)。
1.4 吸附实验取50 mL一定浓度的重金属(Ni2+和Cd2+)溶液模拟重金属废水,置于100 mL具塞锥形瓶中,加入一定量的活性炭,在一定温度和震荡速度下吸附至预定时间,过滤澄清液,使用原子吸收分光光度计在一定波长(Ni2+,232 nm;Cd2+,228.8 nm)下,根据标准曲线测定其浓度。采用公式(1)计算重金属溶液吸附量:
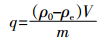
|
(1) |
式中:q为活性炭对重金属离子吸附量(mg·g-1);ρ0为吸附前重金属溶液浓度即初始浓度(mg·L-1);ρe为吸附后重金属溶液浓度即平衡浓度(mg·L-1);V为重金属溶液体积(L);m为投加活性炭的质量(g)。
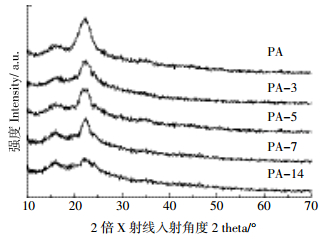
2 结果与讨论 2.1 秸秆青贮过程分析使用XRD考察青贮过程中芦苇秸秆结构的变化,可以得到青贮处理对秸秆结构的影响。图 3为未青贮原料(PA)和分别青贮3、5、7,14 d(PA-3、PA-5、PA-7、PA-14)的X射线衍射谱图。
|
| 图 3 芦苇秸秆及其青贮后的X射线衍射谱图 Figure 3 X-ray diffractogram (XRD) of original PA and silagetreated PA samples |
由图 3所示,不同青贮时间的样品的衍射曲线无明显特征,主要为无定型体的形式存在[14]。在2θ=22.5°处有明显的纤维素的特征峰[15],但是随着青贮时间的增加,特征峰的强度越来越小。这个现象表明,青贮过程破坏了芦苇秸秆原有的结构特征,但它或在失去部分孔道结构的前提下提高了活性剂的利用率和浸渍效果,从而弥补孔道结构的损失。图 4所示芦苇秸秆青贮前后SEM图,更清晰地表明青贮过程破坏了芦苇秸秆的孔结构。表 1所示芦苇原料在青贮过程中元素含量的变化,随着青贮时间的增长,氧元素的含量越来越多,说明芦苇原料中有机酸的积累越来越多。文献[16-17]也证明这一点,并且有机酸的增加主要是由于青贮过程使芦苇秸秆的细胞壁组分和还原糖部分降解所造成。

|
| 图 4 芦苇秸秆(a和c)和青贮7 d后(b和d)的扫描电镜图 Figure 4 SEM micrographs for PA (a and c) and 7 days' silage-treated PA (b and d) |
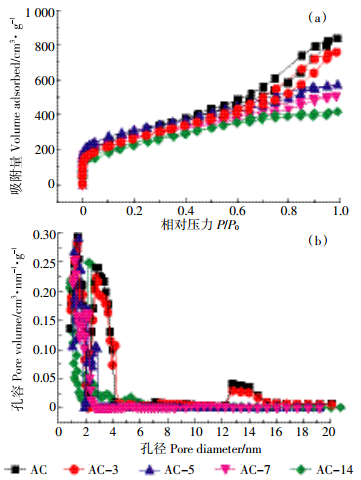
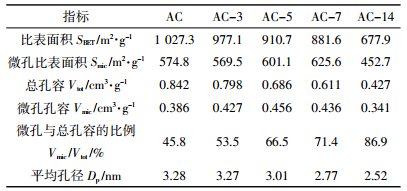
活性炭样品的氮气吸附等温线和孔径分布如图 5所示。在低相对压力(P/P0)条件下,吸附等温线呈现激增趋势,根据国际理论和应用化学联合会(IUPAC)的分类,此处吸附等温线属于Ⅰ型,说明活性炭样品中存在微孔结构。随着P/P0的增加,N2的吸附增加。在P/P0=0.4下,吸附等温线出现了回环,此处吸附等温线属于Ⅳ型,说明活性炭样品中存在介孔结构[18]。表 2为活性炭样品孔径结构的具体参数。随着青贮天数的增加,活性炭样品的比表面积和总孔容逐渐减小,说明在青贮的过程中秸秆原有的孔道结构被破坏,青贮时间越长,孔道破坏的越为严重。也正如图 5所示,随着青贮时间增长,活性炭样品的N2吸附以及等温线中的回环越来越小。但是,活性炭所展现出的微孔比表面积和微孔孔容的比例逐渐增大,图 5b孔径分布图得到同样的结果。由于重金属离子的半径以及水合半径较小(表 3),微孔结构较之介孔大孔更易起到截留作用。所以,青贮活化法制备的活性炭所展现出的微孔结构更利于重金属离子的吸附。
|
| 图 5 活性炭N2吸附等温线(a)和孔径分布(b) Figure 5 N2 adsorption/desorption isotherms (a) and pore distribution (b) of activated carbons |
|
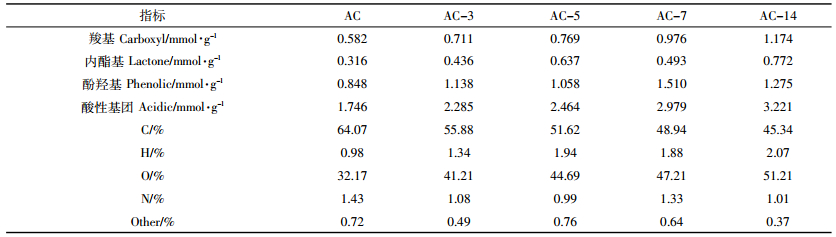
表 4为活性炭样品的Boehm滴定以及元素分析测定结果。青贮活化法制备的活性炭的酸度较普通磷酸活化法有明显提高。随着青贮时间的增长,活性炭的酸度依次增加,其原因由于时间的增长,青贮过程在原料中积累的有机酸增加,故导致活性炭酸度增大。元素分析测定结果显示出同样的趋势,随着青贮时间增长,活性炭中氧元素的含量逐渐增加,含氧官能团通常表现为酸性。所以,青贮活化法可有效提高活性炭表面酸度。
|
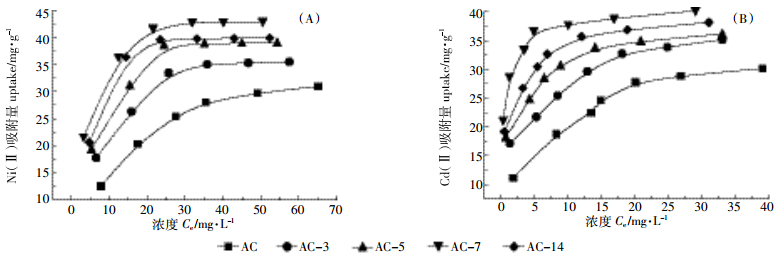
由图 6A和图 6B知,青贮活化法制备的活性炭对重金属离子Ni(Ⅱ)和Cd(Ⅱ)的吸附能力大于普通磷酸法所制备的活性炭,并且随着青贮时间增长,对重金属离子的吸附效果增强,其原因由于青贮活化法制备的活性炭具备较高的酸度以及更多的微孔含量。但是,AC-14反而比AC-7对重金属离子的吸附效果要差,其原因是青贮时间过久导致活性炭的比表面积和孔径含量大幅降低,此现象得出青贮活化法制备高酸度芦苇活性炭的最佳青贮时间,同时印证了文献[19-20]中提出的,活性炭去除重金属离子过程中,表面化学反应起主要作用,而孔径结构次之。
|
| 图 6 不同活性炭样品对Ni(Ⅱ)和Cd(Ⅱ)的吸附效果 Figure 6 Ni (Ⅱ) and Cd (Ⅱ) uptakes of the activated carbons |
在吸附平衡研究中,描述吸附等温线最常用的模型是Langmuir模型和Freundlich模型。Langmuir模型线性表达式为[21]:
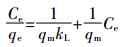
|
(2) |
Freundlich模型线性表达式为[22]:
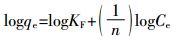
|
(3) |
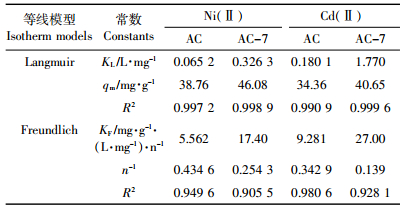
式中:qe为平衡吸附量,mg·g-1;Ce为平衡浓度,mg·L-1;qm为最大吸附量,mg·g-1;KL为Langmuir模型常数;KF和n为Freundlich模型常数。拟合数据计算所得参数如表 5所示,Ni(Ⅱ)和Cd(Ⅱ)的吸附等温线都更接近于Langmuir模型(R2>0.99),这个结果也反映在图 7上。说明该吸附现象为单分子层吸附,即吸附过程发生在吸附剂表面。
|

|
| 实线代表Langmuir模型拟合,虚线代表Freundlich模型拟合 Solid lines represent the Langmuir isotherms and dashed lines represent the Freundlich isotherms 图 7 AC与AC-7的等温线模型拟合 Figure 7 The sorption isotherms of AC and AC-7 |
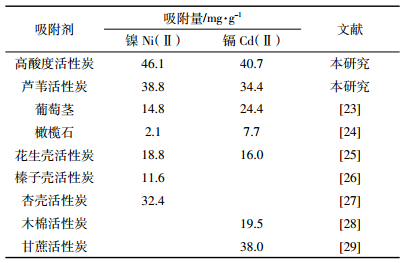
表 6所示,青贮活化法制备的高酸度芦苇活性炭对比其他方法制备活性炭,对于重金属离子Ni(Ⅱ)和Cd(Ⅱ)吸附有明显的效果。也进一步验证了此制备方法的可行性,以及活性炭吸附重金属离子的机理,即化学吸附起主要作用,孔径作用次之[19-20]。
|
研究结果表明,青贮活化法制备高酸度活性炭是一种可行的活性炭制备方法。在制备过程中,随着青贮时间的增长,所制备活性炭的比表面积有所下降,但是微孔比例和活性炭表面酸度有所上升。在原料青贮7 d时,所制备出的活性炭对重金属Ni(Ⅱ)和Cd(Ⅱ)吸附效果最好。吸附等温线研究表明,高酸度活性炭对重金属Ni(Ⅱ)和Cd(Ⅱ)的吸附过程用Langmuir模型可进行很好的描述。高酸度活性炭对重金属离子的吸附过程主要为化学吸附。
利用湿地植物秸秆所制备的活性炭是一种理化性质以及吸附性能较好的吸附剂,而且可以实现以废治废,对于实现农业固废资源化利用具有十分重要意义。青贮活化法为秸秆活性炭的制备提供了新思路和新方法,在实际生产过程中,可以降低生产成本,提高产品性能。今后的研究重点是如何更好地对活性炭进行再生以及实现产品的循环利用。
| [1] | 杨正亮, 冯贵颖, 呼世斌, 等. 水体重金属污染研究现状及治理技术[J]. 干旱地区农业研究, 2005, 23(1): 219–222. YANG Zheng-liang, FENG Gui-ying, HU Shi-bin, et al. Current research trends and controlling technigue for heavy metal pollution in waters[J]. Agricultural Research in the Arid Areas, 2005, 23(1): 219–222. (in Chinese) |
| [2] | 孟多, 周立岱, 于常武. 水体重金属污染现状及治理技术[J]. 辽宁化工, 2006, 35(9): 534–536. MENG Duo, ZHOU Li-dai, YU Chang-wu. Heavy metal pollution of water body and treatment[J]. Liaoning Chemical Industry, 2006, 35(9): 534–536. (in Chinese) |
| [3] | Kobya M, Demirbas E, Senturk E, et al. Adsorption of heavy metal ions from aqueous solutions by activated carbon prepared from apricot stone[J]. Bioresource Technology, 2005, 96: 1518–1521. DOI:10.1016/j.biortech.2004.12.005 |
| [4] | Baccar R, Bouzid J, Feki M, et al. Preparation of activated carbon from Tunisian olive-waste cakes and its application for adsorption of heavy metal ions[J]. Journal of Hazardous Materials, 2009, 162: 1522–1529. DOI:10.1016/j.jhazmat.2008.06.041 |
| [5] | Guo Z, Xu L, Liu C, et al. Comparison of physicochemical properties of activated carbons derived from biomass wastes by H4P2O7 activation:Adsorption of trimethoprim[J]. Desalination and Water Treatment, 2016, 57: 21957–21967. DOI:10.1080/19443994.2015.1127782 |
| [6] | Guo Z, Fan J, Zhang J, et al. Sorption heavy metal ions by activated carbons with well-developed microporosity and amino groups derived from Phragmites australis by ammonium phosphates activation[J]. Journal of the Taiwan Institute of Chemical Engineers, 2016, 58: 290–296. DOI:10.1016/j.jtice.2015.05.041 |
| [7] | 王帅, 商建英, 胡克林, 等. 溶液初始pH值及裂解温度对玉米秸秆基生物炭吸附Cr (Ⅵ) 的影响[J]. 农业资源与环境学报, 2016, 33(5): 443–448. WANG Shuai, SHANG Jian-ying, HU Ke-lin, et al. Impact of initial pH and pyrolysis temperature on the adsorption of Cr (Ⅵ) from aqueous solutions on corn straw-based materials[J]. Journal of Agricultural Resources and Environment, 2016, 33(5): 443–448. (in Chinese) |
| [8] | Liu H, Zhang J, Zhang C, et al. Activated carbons with well-developed microporosity and high surface acidity prepared from lotus stalks by organophosphorus compounds activations[J]. Carbon, 2013, 60: 289–291. DOI:10.1016/j.carbon.2013.04.039 |
| [9] | Liu W, Xie H, Zhang J, et al. Sorption removal of cephalexin by HNO3 and H2O2 oxidized activated carbons[J]. Science China Chemistry, 2012, 55: 1959–1967. DOI:10.1007/s11426-011-4488-3 |
| [10] | Guo Z, Zhang J, Liu H. Ultra-high Rhodamine B adsorption capacities from an aqueous solution by activated carbon derived from Phragmites australis doped with organic acid by phosphoric acid activation[J]. RSC Advances, 2016(6): 40818–40827. |
| [11] | Liu H, Dai P, Zhang J, et al. Preparation and evaluation of activated carbons from lotus stalk with trimethyl phosphate and tributyl phosphate activation for lead removal[J]. Chemical Engineering Journal, 2013, 228: 425–434. DOI:10.1016/j.cej.2013.04.117 |
| [12] | 王寒.玉米秸秆的青贮及水解方法的研究[D].天津:天津大学, 2011. WANG Han. Study on silage and hydrolysis of corn stalk[D]. Tianjin:Tianjin University, 2011. (in Chinese) |
| [13] | 毛磊, 童仕唐, 王宇. 对用于活性炭表面含氧官能团分析的Boehm滴定法的几点讨论[J]. 炭素技术, 2011, 30(2): 17–19. MAO Lei, TONG Shi-tang, WANG Yu. Discussion on the Boehm titration method used in analysis of surface oxygen functional groups on activated carbon[J]. Carbon Techniques, 2011, 30(2): 17–19. (in Chinese) |
| [14] | Liou T H. Development of mesoporous structure and high adsorption capacity of biomass-based activated carbon by phosphoric acid and zinc chloride activation[J]. Chemical Engineering Journal, 2010, 158: 129–142. DOI:10.1016/j.cej.2009.12.016 |
| [15] | Kalia S, Avérous L. Biodegradable and biobased polymers for environmental and biomedical applications[C]. John Wiley & Sons, 2016. |
| [16] | Shultz T A, Ralston A T, Shultz E. Effect of various additives on nutritive value of ryegrass straw silage. Ⅰ: Laboratory silo and in vitro dry matter digestion observations[J]. Journal of Animal Science, 1974, 39: 920–925. DOI:10.2527/jas1974.395920x |
| [17] | Yang X, Chen H, Gao H, et al. Bioconversion of corn straw by coupling ensiling and solid-state fermentation[J]. Bioresource Technology, 2001, 78: 277–280. DOI:10.1016/S0960-8524(01)00024-4 |
| [18] | Rodriguez-Reinoso F, Martin-Martinez J M, Prado-Burguete C, et al. A standard adsorption isotherm for the characterization of activated carbons[J]. Journal of Physical Chemistry, 1987, 91: 515–516. DOI:10.1021/j100287a006 |
| [19] | Cho H, Wepasnick K, Smith B A, et al. Sorption of aqueous Zn[J]. Langmuir, 2010, 26: 967–981. DOI:10.1021/la902440u |
| [20] | Schierz A, Zänker H. Aqueous suspensions of carbon nanotubes:Surface oxidation, colloidal stability and uranium sorption[J]. Environmental Pollution, 2009, 157: 1088–1094. DOI:10.1016/j.envpol.2008.09.045 |
| [21] | Langmuir I. The adsorption of gases on plane surfaces of glass, mica and platinum[J]. Journal of the American Chemical Society, 1918, 40: 1361–1403. DOI:10.1021/ja02242a004 |
| [22] | Freundlich H. Over the adsorption in solution[J]. Journal of Physical Chemistry, 1906, 57: 1100–1107. |
| [23] | Escudero C, Poch J, Villaescusa I. Modelling of breakthrough curves of single and binary mixtures of Cu (Ⅱ), Cd (Ⅱ), Ni (Ⅱ) and Pb (Ⅱ) sorption onto grape stalks waste[J]. Chemical Engineering Journal, 2013, 217: 129–138. DOI:10.1016/j.cej.2012.11.096 |
| [24] | Fiol N, Villaescusa I, Martínez M, et al. Sorption of Pb (Ⅱ), Ni (Ⅱ), Cu (Ⅱ) and Cd (Ⅱ) from aqueous solution by olive stone waste[J]. Separation and Purification Technology, 2006, 50: 132–140. DOI:10.1016/j.seppur.2005.11.016 |
| [25] | Wilson K, Yang H, Seo C W, et al. Select metal adsorption by activated carbon made from peanut shells[J]. Bioresource Technology, 2006, 97: 2266–2270. DOI:10.1016/j.biortech.2005.10.043 |
| [26] | DemirbasšE, Kobya M, Öncel S, et al. Removal of Ni (Ⅱ) from aqueous solution by adsorption onto hazelnut shell activated carbon:Equilibrium studies[J]. Bioresource Technology, 2002, 84: 291–293. DOI:10.1016/S0960-8524(02)00052-4 |
| [27] | Erdoğan S, Önal Y, Akmil-Bašar C, et al. Optimization of nickel adsorption from aqueous solution by using activated carbon prepared from waste apricot by chemical activation[J]. Applied Surface Science, 2005, 252: 1324–1331. DOI:10.1016/j.apsusc.2005.02.089 |
| [28] | Rao M M, Ramesh A, Rao G P C, et al. Removal of copper and cadmium from the aqueous solutions by activated carbon derived from Ceiba pentandra hulls[J]. Journal of Hazardous Materials, 2006, 129: 123–129. DOI:10.1016/j.jhazmat.2005.08.018 |
| [29] | Mohan D, Singh K P. Single-and multi-component adsorption of cadmium and zinc using activated carbon derived from bagasse:An agricultural waste[J]. Water Research, 2002, 36: 2304–2318. DOI:10.1016/S0043-1354(01)00447-X |
 2017, Vol. 34
2017, Vol. 34