文章信息
- 王晓芳, 罗章, 万亚男, 王琪, 孙宏杰, 郭岩彬, 李花粉
- WANG Xiao-fang, LUO Zhang, WAN Ya-nan, WANG Qi, SUN Hong-jie, GUO Yan-bin, LI Hua-fen
- 叶面喷施不同形态硒对草莓吸收和转运硒的影响
- Effects of Foliar-applied Selenite and Selenate on Selenium Accumulation in Strawberry
- 农业资源与环境学报, 2016, 33(4): 334-339
- Journal of Agricultural Resources and Environment, 2016, 33(4): 334-339
- http://dx.doi.org/10.13254/j.jare.2016.0023
-
文章历史
- 收稿日期: 2016-01-14
2. 山东省淄博博山区农业综合开发办公室, 山东 淄博 255200
2. Agricultural Comprehensive Development Office of Boshan, Zibo 255200, China
硒是人体和动物细胞中谷胱甘肽过氧化物酶(GSH-Px)[1]、甲状腺激素脱碘酶[2, 3, 4]和硫氧还蛋白还原酶[5]的必需元素,对人体健康有着十分重要的作用。人体缺硒是克山病和大骨节病等地方病发生、发展的重要环境因素[6]。人体内的硒营养主要来源于植物,土壤中的硒含量状况很大程度上决定了植物硒的含量。但硒在地壳中的含量十分稀少且分散,世界上有2/3的地区属于缺硒地区,我国有72%的县、市存在不同程度缺硒,从东北向西南方向存在一条明显的土壤总硒平均含量约为0.1 mg·kg-1的低硒带[7]。
解决硒营养不足的最重要的途径是强化土壤-植物-动物系统链式传递过程中的各个环节,特别是硒在土壤-植物间的循环与转化环节。很多研究结果表明,通过向土壤中增施Na2SeO4或K2SeO4可以快速提高作物中有效硒含量,而施加亚硒酸盐或者BaSeO4等水溶性较差的外源硒的土壤持续供硒能力较强[8, 9, 10, 11]。芬兰是一个典型的缺硒国家,自1984年官方供用加硒化肥后,各种食物中的硒含量都有了显著提高[12]。叶面喷施硒也能显著提高作物中硒含量[13],叶面喷施是及时调控植物营养状况及微量元素的施用普遍采用的有效方法,叶面喷施的营养物质由于不接触土壤或接触土壤很少而减少了土壤固定,有利于提高营养物质的利用率。本试验选取草莓为试验材料,研究叶面对硒酸钠和亚硒酸钠的吸收与转运,以及草莓果实对不同形态硒的富集规律,为富硒草莓的生产提供技术支持。
1 材料和方法 1.1 试验设置草莓(Fragaria ananassa Duch)田间试验于2013年9月至2015年4月在山东省淄博市博山区上瓦泉村有机富硒草莓采摘园区进行,试验地位于淄博市博山区东南部,属淄博倾斜盆地,海拔高度在400 m以上。土壤类型为褐土,表土质地为中壤和轻壤,土层深厚,通透性好,保肥保水能力强。试验选择了2个草莓大棚,2个试验大棚的土壤基本理化性质见表 1。土壤理化性质详细测定方法参照文献[14],土壤硒背景值参照《土壤和沉积物汞、砷、硒、铋、锑的测定微波消解/原子荧光法》(HJ 680—2013)测定。
供试品种为红颜,选取3叶1心整齐一致、生长健壮的草莓苗进行定植。至草莓初花期进行喷施硒处理,处理方式为叶面喷施,供试硒源为亚硒酸钠(Na2SeO3)、硒酸钠(Na2SeO4),同时设置清水喷施作为对照(CK)。A棚设置硒喷施量为20 g Se·hm-2亚硒酸钠(SeⅣ-20)和硒酸钠(SeⅥ-20) 2个硒处理,试验于2013年9月至2014年4月期间进行;次年根据A棚试验结果,调整硒喷施量在B棚进行进一步硒强化试验,B棚设置硒喷施量为40、60 g Se·hm-2的亚硒酸钠和硒酸钠各2个硒水平,分别为SeⅣ-40、SeⅣ-60和SeⅥ-40、SeⅥ-60。喷施前先将亚硒酸钠和硒酸钠分别配成4 mg Se·mL-1的溶液,根据小区面积和设计喷施量分别取9、18 mL和27 mL相应硒溶液与清水按照1∶500比例稀释后进行叶面喷施。每个处理设置3个重复小区(每4行设为1个小区,小区面积为2 m×9 m),试验小区完全随机排列。试验期间草莓正常栽培管理,果实成熟后分批次采收草莓果实,每批次采收间隔时间约为40 d左右。
1.2 样品处理与分析草莓果实分别于叶面喷施40、80、120 d后进行3次样品采收。选取个体均匀、果实发育充分,无病虫害、无机械伤害、果实表面着色达70%左右的果实采收。每个处理采收草莓果实约1 kg,从中分取一部分,液氮速冻,之后用冷冻干燥设备干燥,磨粉,保存待测。B棚第3次采收草莓果实后,于各个试验小区随机采集5株生长状况良好的草莓植株,洗净晾干,根、茎、叶分别称鲜重、烘干、称干重,粉碎保存待测。
用万分之一天平称取0.250 0 g草莓样品于微波消解管中,加8 mL HNO3(优级纯),遮盖冷消化过夜。第2 d用微波消解仪(CEM,MARS-5)进行微波消解,6 min升温至120 ℃,保持1 min后4 min升温至150 ℃,保持3 min后4 min升温至180 ℃,保持30 min至微波消解完全结束。将消解管中消解液转移至50 mL容量瓶中,用高纯水定容,定量滤纸过滤。取4 mL滤液,加入1 mL 6 mol·L-1 HCl,沸水浴2 h,将试样中的六价硒还原成四价硒,用AFS-920型双道原子荧光光谱仪测定Se(北京吉天仪器有限公司)。在整个样品的测定过程中,采用标准物质圆白菜GBW10014(GSB-5,硒质量分数为0.2±0.03 mg·kg-1)和空白样品进行分析质量控制,标准物质中硒的回收率控制在85%~90%。
1.3 数据处理试验数据为3次重复的平均值和标准误差,采用SPSS软件进行方差分析,应用Microsoft Excel软件进行图表制作。图中数据标识为平均值±标准误差。
2 结果与分析 2.1 不同硒处理对草莓可食部位硒含量的影响在草莓初花期对其叶面喷施亚硒酸钠和硒酸钠均可在短时间内明显提高草莓果实中硒含量,硒施用量越大,草莓样品中硒含量越高(图 1)。A棚中,喷施硒量为20 g Se·hm-2时,喷施亚硒酸钠和硒酸钠的处理第一批草莓样品中硒含量分别是对照组的3倍和5倍。B棚中,硒施用量为40 g Se·hm-2时,喷施亚硒酸钠和硒酸钠的处理第一批草莓样品中硒含量分别是对照组的21倍和24倍;硒施用量为60 g Se·hm-2时,喷施亚硒酸钠和硒酸钠的处理组第一批草莓样品中硒含量分别是对照组的31倍和34倍。

|
| 图中虚线和实线分别表示陕西省富硒食品标准(DB61/T556—2012)中新鲜水果的硒含量指标0.02 mg·kg-1和0.1 mg·kg-1 The dotted line represents concentration of 0.02 mg·kg-1, the solid line represents concentration of 0.1 mg·kg-1 图 1 不同硒处理各批次草莓鲜果中硒含量 Figure 1 Selenium contents in different batches of strawberry |
虽然喷施亚硒酸钠和硒酸钠对提高草莓硒含量的效果没有显著性差异,但硒喷施量相同时,硒酸钠喷施草莓中硒含量在数值上普遍高于亚硒酸钠喷施处理的草莓。施硒量为20 g Se·hm-2时,前两批喷施硒酸钠的草莓样品中硒含量分别比喷施亚硒酸钠的高69.0%和40.0%。施硒量为40 g Se·hm-2时,硒酸钠处理组前两批草莓样品硒含量比亚硒酸钠处理组高15%和30%。施硒量为60 g Se·hm-2时,硒酸钠处理组前两批草莓样品比亚硒酸钠处理组高11%和173%。
在试验设置硒施用量范围内,叶面喷施2种外源硒短期内均可提高草莓可食部位的硒含量,但随着时间延长,草莓可食部位的硒含量快速降低并趋于对照处理(图 1)。对比不同采收批次草莓果实中硒含量的变化可以发现,在低浓度喷施硒的条件下(20 g Se·hm-2),第二批采收的草莓中硒含量就降低到对照处理草莓中的硒含量水平;但在高浓度喷施硒的条件下(40、60 g Se·hm-2),第三批采收的草莓中硒含量还是比对照处理的高。喷施亚硒酸钠时,SeⅣ-20处理第二、三批样品中硒含量与第一批相比分别下降了61%和67%;SeⅣ-40处理第二、三批草莓样品硒含量分别比第一批下降了80%和88%;SeⅣ-60处理第二、三批草莓样品硒含量分别比第一批下降了86%和91%。喷施硒酸钠时,SeⅥ-20组第二、三批样品中硒含量与第一批相比分别下降了68%和81%;SeⅥ-40试验组第二、三批草莓样品硒含量分别比第一批下降了77%和89%;SeⅥ-60试验组第二、三批草莓样品硒含量分别比第一批下降了66%和90%。对于第三批采收的草莓,喷硒处理和对照处理之间硒含量没有显著性差异,说明叶面喷施硒对于提高草莓硒含量见效快,但持续供硒能力较弱。
参照陕西省富硒食品标准(DB61/T 556—2012),鲜水果的硒含量指标0.02~0.1 mg·kg-1,硒施用量为20 g Se·hm-2时,只有第一批草莓鲜果中硒含量达到富硒水果标准。硒施用量为40 g Se·hm-2时,亚硒酸钠和硒酸钠处理第一批草莓鲜果中硒含量略超过富硒水果硒含量指标的上限,第二批达到富硒水果硒含量标准,第三批则低于富硒水果硒含量指标的下限。硒施用量为60 g Se·hm-2时,亚硒酸钠和硒酸钠处理第一批草莓样品中硒含量超过富硒水果硒含量指标的上限,第二批达到富硒水果硒含量标准,第三批也低于富硒水果硒含量指标的下限。喷施结果表明,随着硒喷施量的增加,各批次草莓鲜果中硒的含量也相应有所增加。但随着草莓的生长,后期采收的草莓鲜果中硒含量可能达不到富硒水果硒含量指标的下限,实际生产过程中可以对施硒量或者施硒次数进行科学合理的调整。
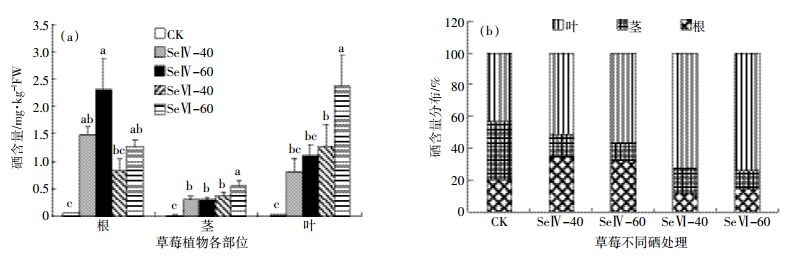
2.2 不同硒处理对草莓植株各部位吸硒量以及硒在草莓植株中分布的影响叶面喷硒4个月后,各处理草莓植株各部位硒含量均高于对照组(图 2(a))。喷硒处理草莓根中硒含量是对照处理的14~38倍,相同硒浓度下,亚硒酸钠处理根中硒含量较高,约为硒酸钠处理的1.8倍;喷硒处理草莓茎中硒含量是对照处理的28~50倍,但不同硒处理之间差异不显著;喷硒处理草莓叶片中硒含量也显著高于对照处理,约为对照处理的34~100倍。
|
| 图 2 不同硒处理草莓根、茎、叶各部位硒含量(a)及分布(b) Figure 2 Se concentration (a) and distribution (b) in roots, stems and leaves of strawberry with different treatments |
此外,不同硒处理草莓根、茎、叶各部位硒含量分布也有显著差异(图 2(b))。对照组根茎叶各部位硒含量所占百分比差异不大,亚硒酸钠处理组(SeⅣ-40和SeⅣ-60)根部硒所占百分比为33%~35%,茎中硒所占百分比为11%~14%,叶片中硒所占百分比为51%~57%;硒酸钠处理组(SeⅥ-40和SeⅥ-60)根部硒所占百分比为12%~14%,茎中硒所占百分比为12%~15%,叶片中硒所占百分比为72%~74%。在亚硒酸钠处理组,叶片所吸收的硒约50%累积在叶片中,约30%转移到根部,茎作为硒的转运通道含量最少;在硒酸钠处理组,叶片所吸收的硒约70%累积在叶片中,根和茎中含量均较少。
3 讨论亚硒酸盐和硒酸盐是可以被植物根系吸收的两个主要形态的硒,与根系相比,植物叶片具有直接快速吸收营养物质并运往其他组织器官的能力[15, 16]。诸多研究表明,硒被植物叶片吸收后可以向植物其他器官转移,对菊苣菜幼叶进行叶面喷硒,成熟期后其顶部叶片中的硒含量是空白对照的两倍[17]。Poggi等[18]对土豆进行叶面喷硒,结果发现叶面喷亚硒酸钠和硒酸钠均可显著提高土豆块茎中的硒含量,且土豆块茎中的硒含量随着叶面喷硒量增加而增加。Nawaz[19]对小麦进行不同外源硒处理,结果发现叶面喷施的效果要优于基施硒肥和拌种。Smrkolj等[20]对大豆的研究也表明硒使用量相同时,在花期对大豆进行叶面喷硒处理,收获的大豆种子中硒含量要高于浸种处理。本试验结果也表明在试验浓度范围内于草莓初花期进行叶面喷施硒可以在短期内快速提高草莓果实的硒含量。
本试验结果表明施硒量相同时硒酸钠处理草莓中硒的含量高于亚硒酸钠处理,即硒酸钠对提高草莓果实中硒含量的效果优于亚硒酸钠。王其兵等[21]对花生的研究表明,叶片对亚硒酸盐和硒酸盐两种形态的硒化合物均能吸收利用并转移至植物体的其他部位,但对这两种价态硒的吸收富集能力不同。Hu等[22]对水稻进行叶面喷施硒的结果也发现,喷施硒酸钠的水稻籽粒硒含量比喷施亚硒酸钠的高出35.9%,这也证实了施用硒酸盐对增加作物含硒量具有更高的有效性。此外,本试验中叶面喷施亚硒酸钠后4个月,约有30%~35%的硒转移到了根部,而硒酸钠从叶片转移到根部的硒不到15%。茎作为硒从叶片转移到根部的必经通道,各处理茎中硒含量基本相同约占植株总硒量的10%至15%。植物叶片吸收的营养物质在叶片中经过代谢转化后以有机物的形式通过韧皮部运输到根部,因此,草莓对硒酸钠和亚硒酸钠的吸收富集差异以及硒酸钠和亚硒酸钠在草莓植株内分布差异可能是由于四价硒和六价硒在植物体内代谢差异造成的。
目前关于硒在植物体内的转运和代谢机制,多数研究认为由于硒和硫为同族元素,原子大小几乎相同,其键能、电离性质、电子亲和力和电负性也相近,所以推测高等植物同化硒的途径与同化硫的途径基本相同。Rotte等[23]研究发现了质粒中硫酸盐的代谢途径,Sors等[24]根据相关研究结果推测硒酸盐以SeO42-的形式进入植物叶片中的叶绿体,在ATP硫酸化酶和APS还原酶的作用下被还原成四价硒,四价硒在半胱氨酸合成酶、硒代蛋氨酸甲基转移酶等多种酶的作用下变成多种有机态的硒。这些有机态的硒或储存于植物叶片中或转移到植物其他器官,一部分有机态硒随植物叶片中其他营养物质一起通过韧皮部运输到植物根部。四价硒进入植物体中可以很快地转化为各种有机硒形态,而六价硒进入植物体转化为有机形态的速率比四价硒低[25]。在硒同化的过程中,六价硒需要先被还原成四价硒再被有机化,而四价硒则可以直接被有机化,可见六价硒在植物叶片中的同化代谢比四价硒慢,受此同化过程的影响,植物叶片吸收的六价硒向根部转移也相对较慢,在相同时间内转移的量也更少。
4 结论在草莓初花期进行叶面喷施亚硒酸钠或硒酸钠短期内均可显著提高草莓鲜果中硒的含量,随着硒喷施量的增加,草莓鲜果中硒的含量显著提高,但是叶面喷施的硒持续供给果实的能力有限,随着草莓果实的连续生长,后期采收的草莓中硒含量显著下降。进行叶面喷硒后,叶片吸收的亚硒酸钠更容易向根部转移,而硒酸钠则更多的累积于叶片中。
本试验结果表明硒酸钠对于提高草莓果实硒含量的效果略优于亚硒酸钠,但考虑到硒酸钠的毒性和环境风险较大,建议实际生产中使用亚硒酸钠对草莓进行硒生物强化,同时,为了避免硒与草莓果实的直接接触,建议草莓在初花期进行叶面喷施,不要在草莓结果时补硒;在草莓初花期每公顷喷施20~40 g硒时,早期草莓果实硒含量可达到富硒食品标准DB61/T 556—2012中新鲜水果的硒含量指标。
| [1] | Rotruck J T, Pope A L, Ganther H E, et al. Selenium:biochemical role as a component of glutathione peroxidase[J]. Science, 1973,179(4073):588-590. |
| [2] | Berry M J, Banu L, Chen Y Y, et al. Recognition of UGA as a selenocysteine codon in type 1 deiodinase requires sequences in the 3' untranslated region[J]. Nature, 1991,353(6341):273-276. |
| [3] | Ramauge M, Pallud S, Esfandiari A, et al. Evidence that type Ⅲ iodothyronine deiodinase in rat astrocyte is a selenoprotein[J]. Endocrinology, 1996,137(137):3021-3025. |
| [4] | Pallud S, Lennon A M, Ramauge M, et al. Expression of the type II iodothyronine deiodinase in cultured rat astrocytes is selenium-dependent[J]. Journal of Biological Chemistry, 1997, 272(29):18104-18110. |
| [5] | Tamura T, Stadtman T C. A new selenoprotein from human lung adenocarcinoma cells:purification, properties, and thioredoxin reductase activity[J]. Proceedings of the National Academy of Sciences of the United States of America, 1996, 93(3):1006-1011. |
| [6] | 中国科学院地理研究所环境与地方病研究组. 我国低硒带与克山病、大骨节病病因关系的研究[J]. 环境科学, 1986, 7(4):89-93. Research Team of Environment and Endemic Diseases. Studies on low selenium belt in China and pathogeny of Keshan and Kaschin-beck diseases[J]. Chinese Journal of Environmental Science, 1986, 7(4):89-93. (in Chinese) |
| [7] | 中国科学院地理研究所化学地理研究室环境与地方病组. 我国克山病病带与非病带发硒分布的地理规律[J]. 地理学报, 1982, 37(2):136-143. Environment and Endemic Disease Section, Institute of Geography, Chinese Academy of Sciences. Geographical distribution of selenium content in human hair in Keshan-disease and non-disease zones in China[J]. Acta Geographica Sinica,1982, 37(2):136-143. (in Chinese) |
| [8] | Broadley M R, White P J, Bryson R J, et al. Biofortification of UK food crops with selenium[J]. Proceedings of the Nutrition Society, 2006, 65(2):169-181. |
| [9] | Combs G F. Selenium in global food systems[J]. British Journal of Nutrition, 2001, 85(5):517. |
| [10] | Gissel Nielsen G. Effects of selenium supplementation of field crops.[M]//Frankenberger W T, Engberg R A, et al. Environmental chemistry of selenium, New York:Marcel Dekker, 1998:99-112. |
| [11] | Gupta U C, Gupta S C. Quality of animal and human life as affected by selenium management of soils and crops[J]. Communications in Soil Science and Plant Analysis, 2002,33(15-18):2537-2555. |
| [12] | Ekholm P, Reinivuo H, Mattila P, et al. Changes in the mineral and trace element contents of cereals, fruits and vegetables in Finland[J]. Journal of Food Composition and Analysis, 2007, 20(6):487-495. |
| [13] | Ducsay L, Lozek O. Effect of selenium foliar application on its content in winter wheat grain[J]. Plant Soil & Environment, 2006,52(2):78-82. |
| [14] | 鲍士旦. 土壤农化分析(第三版)[M]. 北京:中国农业出版社, 2005. BAO Shi-dan.Soil agro-chemistrical analysis(third edition)[M]. Beijing:China Agricultural Press, 2005. (in Chinese) |
| [15] | Neumann P M. Plant growth and leaf-applied chemicals[M]. Boca Raton, Florida:CRC Press, 1988. |
| [16] | Peuke A D, Jeschke W D, Dietz K J, et al. Foliar application of nitrate or ammonium as sole nitrogen supply in Ricinus communis:I. Carbon nitrogen uptake inflows[J]. New Phytologist, 2008,138(4):675-687. |
| [17] | Germ M, Stibilj V, Osvald J, et al. Effect of selenium foliar application on chicory[J]. Journal of Agricultural and Food Chemistry, 2007, 55(3):795-798. |
| [18] | Poggi V, Arcioni A, Filippini P, et al. Foliar application of selenite and selenate to potato[J]. Journal of Agricultural and Food Chemistry, 2000,48(10):4749-4751. |
| [19] | Nawaz F, Ashraf M Y, Ahmad R, et al. Supplemental selenium improves wheat grain yield and quality through alterations in biochemical processes under normal and water deficit conditions[J]. Food Chemistry, 2015,175:350-357. |
| [20] | Smrkolj P, Osvald M, Osvald J, et al. Selenium uptake and species distribution in selenium-enriched bean(Phaseolus vulgaris L.) seeds obtained by two different cultivations[J]. European Food Research and Technology, 2007,225(2):233-237. |
| [21] | 王其兵, 李凌浩, 邢雪荣. 植物叶片对硒的吸收与转运[J]. 植物学通报, 1995(S2):149-155. WANG Qi-bing, LI Ling-hao, XING Xue-rong. Selenium uptake and transporting by plant leaves[J]. Chinese Bulletin of Botany, 1995(S2) 149-155. (in Chinese) |
| [22] | Hu Q, Chen L, Xu J, et al. Determination of selenium concentration of rice in China and effect of fertilization of selenite and selenate on selenium content of rice[J]. Journal of Agricultural & Food Chemistry, 2002, 50(18):5128-5130. |
| [23] | Rotte C, Leustek T. Differential subcellular localization and expression of ATP sulfurylase and 5'-adenylylsulfate reductase during ontogenesis of Arabidopsis leaves indicates that cytosolic and plastid forms of ATP sulfurylase may have specialized functions[J]. Plant Physiol, 2000, 124:715-724. |
| [24] | Sors T G, Ellis D R, Salt D E. Selenium uptake,translocation, assimilationand metabolic fate in plants[J]. Photosynthesis Research, 2005, 86:373-389. |
| [25] | Li H F, McGrath S P, Zhao F J. Selenium uptake, translocation and speciation in wheat supplied with selenate or selenite[J]. New Phytologist, 2008, 178(1):92-102. |
 2016, Vol. 33
2016, Vol. 33