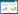文章信息
- 刘青松, 赵丽芳
- LIU Qing-song, ZHAO Li-fang
- 热解温度对生物炭表面性质及释放氮磷的影响
- Effects of Biochar Pyrolysis Temperature on Its Surface Characteristics and Nitrogen and Phosphorus Release
- 农业资源与环境学报, 2016, 33(2): 164-169
- Journal of Agricultural Resources and Environment, 2016, 33(2): 164-169
- http://dx.doi.org/10.13254/j.jare.2015.0256
-
文章历史
- 收稿日期: 2015-10-27
生物炭是生物质在厌氧或缺氧条件下热解产生的富含碳质的产物[1]。生物质一般由纤维素、半纤维素和木质素构成,在热解过程中某些化学键断裂,在表面形成一些官能团,如羟基-OH、芳香性CH、酮基C=O和芳香性C=C键等。近年来,生物炭作为改良剂增强土壤肥力引起了人们的广泛关注[2, 3, 4, 5, 6]。有观点认为,生物炭增加作物产量是因为它提高土壤矿质营养的生物有效性或提供部分矿质营养,从而促进作物的生长。陈心想等[7]发现,施用生物炭可有效增加土壤的矿质氮、有效磷含量,增幅分别为6%~112.8%和3.8%~38.5%。王艳红等[8]发现,稻壳基生物炭对土壤有效磷的提升作用明显。Wang等[9]研究表明桉木与动物粪便混合制备的生物炭含P丰富,可以提高土壤的肥力。Yao等[10]将多种生物炭应用于沙土,发现某生物炭在减少硝态氮、氨氮溶出的同时,增加了磷的溶出。
生物炭的营养元素含量与生物质种类及制备条件有关。纤维素在干木中含量为40%~50%,半纤维素在干木中的含量为25%~35%,木质素在木材和草本植物中的含量分别为20%~40%和10%~40%[11]。生物质的热解反应依赖于热解温度,不同组分的分解程度随温度变化,从而导致生物炭组成及性质的变化。目前,人们对热解温度影响生物炭表面性质的理解还不深入,对热解温度影响生物炭氮磷释放的研究尚未见诸报道。
本研究选取玉米秸秆和杨木2种生物质,在250~450℃范围内热解制备生物炭,采用X-射线光电子能谱仪(XPS)和傅里叶变换红外分析仪(FTIR)研究生物炭的表面元素、基团组成。由于土壤体系影响因素复杂,本研究仅关注生物炭在水溶液中的N、P释放行为,研究NH4+-N、NO3--N、总磷(TP)的等温释放效果以及释放动力学,揭示热解温度对生物炭N、P释放的影响,为进一步地研究生物炭对土壤矿质营养的影响提供参考。
1 材料与方法 1.1 生物炭的制备将成熟期玉米秸秆和杨木嫩枝反复洗涤,在80℃下烘干,冷却至室温,用高速粉碎机破碎,过20目筛。称取10.0 g过筛粉末,分别于250、350、400、450℃温度下,在马弗炉内热解2 h,升温速率4℃·min-1,完成后自然冷却,制备的生物炭密封保存。依据热解温度,玉米秸秆生物炭标记为CB250、CB350、CB400和CB450,杨木生物炭标记为PB250、PB350、PB400和PB450。
1.2 生物炭的表征 1.2.1 X-射线光电子能谱分析(XPS)仪器为美国物理电子公司的PHI 5700 ESCA System。采用条件:铝靶(1 486.6 eV)辐照样品激发光电子,半球型精密电子能量分析器,首先采集样品在0~1 200 eV进行全谱扫描,通过能为187.85 eV。而后采集不同元素轨道的精密扫描,通过能为29.35 eV。
1.2.2 傅里叶变换红外分析(FTIR)采用日本岛津公司生产的IRPvestige-21傅里叶变换红外光谱仪。测试条件:波数范围为400~4 000 cm-1。取适量干燥生物炭与无水KBr一起在玛瑙研钵中碾磨、混合均匀,压片制样后测定生物炭红外光谱图,随后分析其官能团种类。
1.2.3 热重分析(TG/DTG)称取在105℃下烘至恒重的样品,用ZRY-2P综合热分析仪进行热重分析。
1.3 氮、磷的等温释放分别取各生物炭样品0.100 g置于250 mL三角瓶,加入100 mL去离子水,以120 r·min-1的频率恒温(25℃)振荡72 h,过滤,测定滤液中NH4+-N、NO3--N和TP浓度,每个处理重复5次。NH4+-N采用纳氏试剂法,NO3--N采用紫外分光光度法,TP采用钼锑抗分光光度法[12]。NH4+-N、NO3--N和TP的释放量用下式计算:
Q=V×C/m
式中:Q—各物质的释放量(mg·kg-1);V—溶液体积(mL);C—各种物质在溶液中的浓度(mg·mL-1);m—生物炭样品的质量(kg)。
1.4 氮、磷释放动力学对每种生物炭,称取多组同量样品(0.100 g)加入100 mL去离子水,形成系列平行样品。以120 r·min-1的频率振荡(25℃),分别在3、6、12、24、48 h和72 h分离、取样,测定滤液中NH4+-N、NO3--N和TP浓度,释放速率使用公式Qt /Qe计算得到。Qt表示不同时刻各物质的释放量,Qe表示平衡时各物质的释放量。
1.5 数据处理与统计采用Excel 2010和SPSS 16.0软件对试验数据进行处理,应用Duncan多重比较进行差异显著性分析。
2 结果与讨论 2.1 生物炭表面特性 2.1.1 表面元素组成根据XPS分析得到的生物炭表面元素组成如表 1、表 2所示。对于CB生物炭,随着热解温度的升高,碳含量逐渐降低,氧含量则逐渐增加,说明热解中碳的损失较氧更严重。对于氮含量,CB400最高而CB450最低,表明450℃下含氮基团大量分解。对于磷含量,随着热解温度升高先增加后降低,CB350最大。O/C反映生物炭亲水性的强弱[13]。O/C从CB250的0.25逐渐增加到CB450的0.34,说明CB生物炭亲水性逐渐增强,也反映含氧官能团数量增加。极性指数(N+O)/C表征生物炭极性的强弱[14]。(N+O)/C从CB250的0.27上升到CB450的0.35,说明生物炭极性逐渐增强。
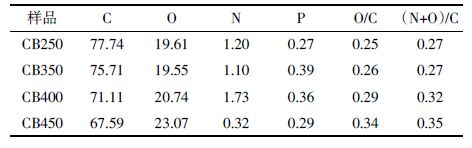
对于PB生物炭,热解温度从250℃升高到400℃,碳含量略有上升、氧含量略有下降,但是变化幅度不大。对于氮含量,PB350最高而PB400、PB450较低,也反映含氮基团在高温下的分解。磷含量首先升高,PB400达到最大值,而PB450有明显下降。热解温度从250℃升高到400℃,PB生物炭的O/C和(N+O)/C呈现下降趋势,表明其亲水性与极性有所减弱,与CB生物炭的变化规律相反。
2种生物炭相比,CB生物炭含碳量更低、含氧量更高,主要与2种生物质的元素组成相关。O/C和(N+O)/C 2个参数,CB系列也明显高于PB系列,反映它们的亲水性、极性以及表面官能团存在明显差别。综合以上结果,生物炭的表面元素组成,既与生物质种类有关,也与热解温度密切相关。
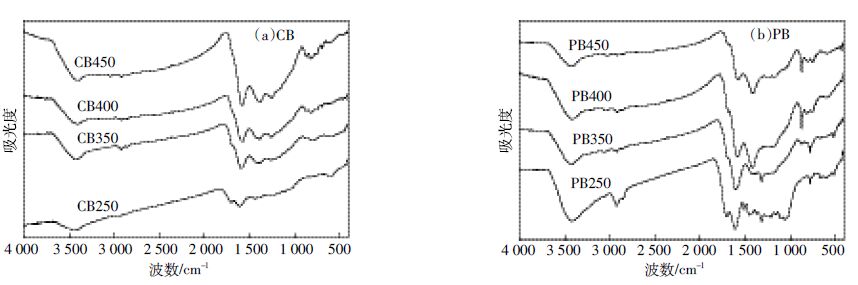
2.1.2 FTIR分析图 1为生物炭的红外光谱图。从图 1可以看出,2种生物炭的主要吸收峰类似。3 400~3 420 cm-1的吸收峰对应-OH的伸缩振动。2 850~2 847 cm-1的吸收峰对应脂肪族-CH的振动,随着热解温度的升高,该吸收峰有减弱的趋势。在热解温度较低时(250℃),1 700~1 710 cm-1出现较弱吸收峰,对应COOH的振动,该峰随热解温度的升高而消失。1 580~1 620 cm-1范围内的较强吸收峰对应C=O的振动[15],表明生物炭中C=O基团增多。在较高的热解温度下,2种生物炭在1 390~1 410 cm-1范围内出现新的吸收峰并有向低波移动的趋势,对应芳香性-CH2的振动,表明生物炭的芳香性逐渐增强。
|
| 图 1 生物炭的FTIR 谱图 Figure 1 FTIR spectra of the biochars |
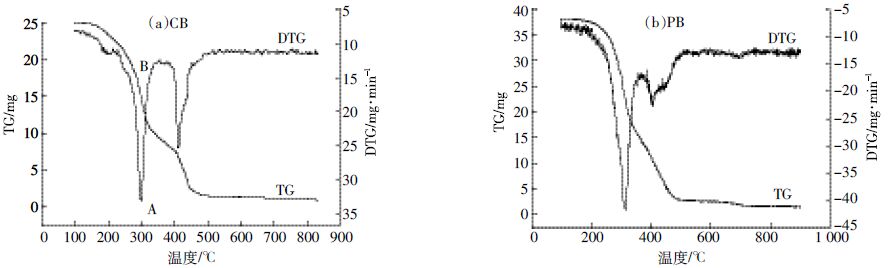
图 2为玉米秸秆和杨木2种生物质的热重分析结果。TG曲线反映加热中生物质质量随着温度的变化,DTG曲线反应生物质失重速率随温度的变化。可以看出,2种生物质的失重速率有2个明显的峰值。在300℃附近出现第1个失重峰,主要对应挥发分及半纤维素的裂解过程;在400℃附近出现第2个失重峰,主要对应纤维素的裂解过程[16]。木质素的分解在较宽的温度范围内进行(200~500℃)。
|
| 图 2 生物质的热重分析图 Figure 2 DTG/TG analysis of biomass |
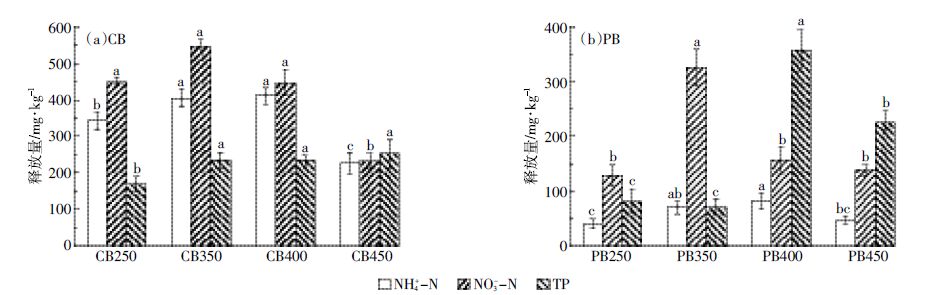
生物炭释放NH4+-N、NO3--N和TP的效果如图 3所示。随着热解温度的升高,2种生物炭的NH4+-N和NO3--N释放量均表现先增大后减小的趋势,这与表面元素分析发现氮元素含量在高温降低相一致。对于CB生物炭,热解温度从250℃升高到350℃,NH4+-N释放量显著增加;从400℃升高到450℃,NH4+-N释放量显著下降。CB400的NH4+-N释放量最大,为411.1 mg·kg-1。CB生物炭的NO3--N释放量,在热解温度从400℃升高到450℃时出现显著下降。CB350的NO3--N释放量最大,为546.0 mg·kg-1。对于PB生物炭,NH4+-N释放量在热解温度从250℃升高到350℃时显著上升,从400℃升高到450℃显著下降。NH4+-N释放量最大的是PB400,为81.6 mg·kg-1。PB生物炭NO3--N释放量的变化趋势与NH4+-N相同,最大的是PB350,为326.4 mg·kg-1。对于CB生物炭,其NH4+-N和NO3--N的释放量无显著差异(P>0.05);对于PB生物炭,其NO3--N的释放量显著高于NH4+-N(P<0.01),说明2种生物炭中氮的形态分布存在差异。计算NH4+-N和NO3--N释放量之和,CB250、CB350、CB400和CB450分别为792.3、950.9、858.6 mg·kg-1和459.0 mg·kg-1,PB250、PB350、PB400和PB450分别为168.6、395.7、237.9 mg·kg-1和185.4 mg·kg-1,也表现出随温度升高先增大后减小的趋势。2种生物炭相比,相同热解温度下,CB释放NH4+-N和NO3--N的总量显著高于PB(P<0.01)。Mukherjee等[17]以橡木、松木和草为原料,在250、650 ℃温度下制备生物炭,发现其在水中的总氮释放量为23~635 mg·kg-1。可见,生物炭释放NH4+-N、NO3--N的量,既取决于生物质种类,也与热解温度有关。
|
| 同一释放物小写字母不同代表差异显著(P<0.05) Lower case letters for the same matter suggest significant difference frombiochars(P<0.05) 图 3 生物炭释放NH4+-N、NO3--N 和TP Figure 3 The release of NH4+-N, NO3--N and TP |
对于TP的释放,2种生物炭的表现存在明显差别。CB250的TP释放量为168.9 mg·kg-1,热解温度升至350 ℃释放量显著增加(P<0.05),继续升高变化不大(P>0.05),CB450的释放量为252.7 mg·kg-1。PB250、PB350的TP释放量较低,但是随着热解温度升高到400℃,TP释放迅速增加(P<0.05),PB400的释放量达到357.4 mg·kg-1;热解温度升至450 ℃后,TP释放又出现显著下降(P<0.05)。结合生物炭表面元素分析的结果,在TP释放与磷的表面含量之间不存在明显相关关系。原因可能在于,生物炭中的磷存在正磷酸、焦磷酸、与芳环相连的磷等形态[18],各形态的磷释放到水中的难易程度不同。Wang等[19]研究表明,400℃热解制备的家禽粪便基生物炭的TP释放量约为170 mg·kg-1。Qian等[20]研究表明,稻壳基生物炭在水中的TP释放量约为2 200 mg·kg-1。Mukherjee等[17]研究表明,橡木、松木和草制备生物炭的TP释放量为46~1 664 mg·kg-1。可见,生物炭的TP释放量也与生物质种类及热解温度相关。
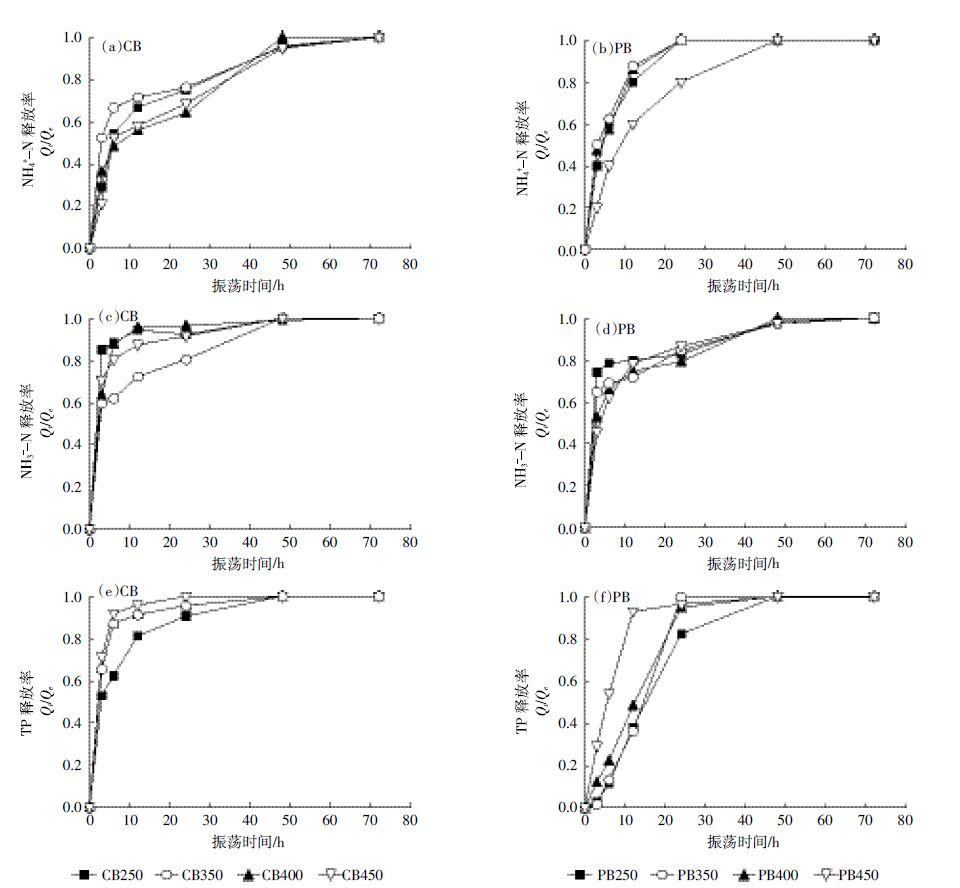
2.3 氮、磷释放动力学对生物炭释放NH4+-N、NO3--N和TP的动力学进行了研究,结果如图 4所示。图 4(a)、4(b)为CB、PB释放NH4+-N动力学。在释放初期阶段,NH4+-N含量较低的生物炭释放的相对速率更慢。对于各生物炭,NH4+-N的释放在48 h内基本完成。图 4(c)、4(d)为CB、PB释放NO3--N动力学。可以看出,与NH4+-N相比,NO3--N的释放更快,尤其在初期的差别更明显。这种现象的原因可能有2个:(1)NO3--N是易溶组分,易于释放;(2)生物炭表面带负电荷,与NH4+-N之间的静电引力作用降低了其释放速率。图 4(e)、4(f)为CB、PB释放TP动力学。可以发现,CB释放TP的相对速率较快,前3 h释放比例已经超过50%。PB释放TP的相对速率较慢,在较长时间内的释放比例不高,表明两种生物炭中磷的存在形态存在差别。总体而言,在48 h内生物炭释放NH4+-N、NO3--N和TP基本完成。
|
| 图 4 生物炭NH4+-N、NO3--N 和TP释放动力学 Figure 4 The release kinetics of NH4+-N, NO3--N and TP from biochars |
生物炭表面元素分析表明,随着热解温度的升高,CB生物炭的含碳量降低、含氧量升高,而PB生物炭的碳、氧含量变化不大;2种生物炭的氮、磷含量都表现出先升高、后降低的趋势;CB生物炭的极性、亲水性增强,而PB生物炭则相反。FTIR分析表明生物炭含有较多的C=O基团,芳香性增强。随着热解温度的升高,生物炭释放NH4+-N、NO3--N的数量先增加后减少。CB生物炭的TP释放量有所增加,而PB的TP释放量先增加后降低。NH4+-N、NO3--N释放与表面氮元素含量之间存在关联,而TP释放与表面磷元素含量之间没有明确关系。生物炭的NH4+-N、NO3--N和TP释放较快,在48 h内基本完成,但是在初期不同生物炭的释放速率存在差别。热解温度在很大程度上影响生物炭的氮磷释放行为。
| [1] | 卜晓莉, 薛建辉. 生物炭对土壤生境及植物生长影响的研究进展[J]. 生态环境学报, 2014, 23(3):535-540. BU Xiao-li, XUE Jian-hui. Biochar effects on soil habitat and plant growth:A review[J]. Ecology and Environmental Sciences, 2014, 23(3):535-540.(in Chinese) |
| [2] | Mukherjee A, Zimmerman A R, Harris W. Surface chemistry variations among a series of laboratory-produced biochars[J]. Geoderma, 2011, 163(3-4):247-255. |
| [3] | 曾爱, 廖允成, 张俊丽, 等. 生物炭对土土壤含水量、有机碳及速效养分含量的影响[J]. 农业环境科学学报, 2013, 32(5):1009-1015. ZENG Ai, LIAO Yun-cheng, ZHANG Jun-li, et al. Effects of biochar on soil moisture, organic carbon and available nutrient contents in manural loessial soils[J]. Journal of Agro-Environment Science, 2013, 32(5):1009-1015.(in Chinese) |
| [4] | 张晗芝, 黄云, 刘钢, 等. 生物炭对玉米苗期生长、养分吸收及土壤化学性状的影响[J]. 生态环境学报, 2010, 19(11):2713-2717. ZHANG Han-zhi, HUANG Yuan, LIU Gang, et al. Effects of biochar on corn growth, nutrient uptake and soil chemical properties in seeding stage[J]. Ecology and Environmental Sciences, 2010, 19(11):2713-2717.(in Chinese) |
| [5] | 王萌萌, 周启星. 生物炭的土壤环境效应及其机制研究[J]. 环境化学, 2013, 32(5):768-780. WANG Meng-meng, ZHOU Qi-xing. Study on the soil environmental effects of biochar and the mechanism[J]. Environmental Chemistry, 2013, 32(5):768-780.(in Chinese) |
| [6] | 张广恪, 邓春生, 张燕荣. 生物炭对土壤拦截外源氮磷等污染物效果的影响[J]. 农业环境科学学报, 2015, 34(9):1782-1789. ZHANG Guang-ke, DENG Chun-sheng, ZHANG Yan-rong. Effect of biochar on interception of sewage nitrogen, phosphorus and COD[J]. Journal of Agro-Environment Science, 2015, 34(9):1782-1789.(in Chinese) |
| [7] | 陈心想, 何绪生, 耿增超, 等. 生物炭对不同土壤化学性质、小麦和糜子产量的影响[J]. 生态学报, 2013, 33(20):6534-6542. CHEN Xin-xiang, HE Xu-sheng, GENG Zeng-chao, et al. Effects of biochar on selected soil chemical properties and on wheat and millet yield[J]. Acta Ecological Sinica, 2013, 33(20):6534-6542.(in Chinese) |
| [8] | 王艳红, 李盟军, 唐明灯, 等. 稻壳基生物炭对生菜Cd吸收及土壤养分的影响[J]. 中国生态农业学报, 2015, 23(2):207-214. WANG Yan-hong, LI Meng-jun, TANG Ming-deng, et al. Effect of rice husk biochar on lettuce Cd uptake and soil fertility[J]. Chinese Journal of Eco-Agriculture, 2015, 23(2):207-214.(in Chinese) |
| [9] | Wang T, Campus-Arbestain M, Hedley M. The fate of phosphorus of ash-rich biochars in a soil-plant system[J]. Plant Soil, 2014, 375(1-2):61-74. |
| [10] | Yao Y, Gao B, Zhang M, et al. Effect of biochar amendment on sorption and leaching of nitrate, ammonium, and phosphate in a sandy soil[J]. Chemosphere, 2012, 89(11):1467-1471. |
| [11] | Mohan D, Pittman C U, Steele P H. Pyrolysis of wood/biomass for bio-oil:A critical review[J]. Energy and Fuels, 2006, 20:848-889. |
| [12] | 国家环境保护总局. 水和废水监测分析方法(第四版)[M]. 北京:中国环境科学出版社, 2002. Chinese NEPA. Water and wastewater monitoring methods(4th edition)[M]. Beijing:Chinese Environmental Science Publishing House, 2002.(in Chinese) |
| [13] | 黄华, 王雅雄, 唐景春, 等. 不同烧制温度下玉米秸秆生物炭的性质及对萘的吸附性能[J]. 环境科学, 2014, 35(5):1884-1890. HUANG Hua, WANG Ya-xiong, TANG Jing-chun, et al. Properties of maize stalk biochar produced under different pyrolysis temperatures and its sorption capability to naphthalene[J]. Environmental Science, 2014, 35(5):1884-1890.(in Chinese) |
| [14] | Nelson N O, Agudelo S C, Yuan W, et al. Nitrogen and phosphorus availability in biochar-amended soils[J]. Soil Science, 2011, 176(5):218-226. |
| [15] | 程国淡, 黄青, 张凯松. 热解温度和时间对生物干化污泥生物炭性质的影响[J]. 环境工程学报, 2013, 7(3):1133-1138. CHENG Guo-dan, HUANG Qing, ZHANG Kai-song. Effect of temperature and duration of pyrolysis on properties of bio-dried sludge biochar[J]. Chinese Journal of Environmental Engineering, 2013, 7(3):1133-1138.(in Chinese) |
| [16] | Yang H P, Yan R, Chen H, et al. Characteristics of hemicellulose, cellulose and lignin pyrolysis[J]. Fuel, 2007, 86(12-13):1781-1788. |
| [17] | Mukherjee A, Zimmerman A R. Organic carbon and nutrient release from a range of laboratory-produced biochars and biochar-soil mixtures[J]. Geoderma, 2013, 193-194:122-130. |
| [18] | 钱婷婷. 磷在固体废物热处理过程中的迁移转化及再利用[D]. 合肥:中国科学技术大学, 2014:58-60. QIAN Ting-ting. Transformation behavior of phosphorus during the thermal treatment of solid wastes and its utilization[D].Hefei:University of Science and Technology of China, 2014:58-60.(in Chinese) |
| [19] | Wang Y, Lin Y, Chiu P C, et al. Phosphorus release behaviors of poultry litter biochar as a soil amendment[J]. Science of the Total Environment, 2015, 512-513:454-463. |
| [20] | Qian T, Zhang X, Hu J, et al. Effects of environmental conditions on the release of phosphorus from biochar[J]. Chemosphere, 2013, 93:2069-2075. |
 2016, Vol. 33
2016, Vol. 33